
【题目】下列有关物质的性质和用途具有对应关系的是
A.SO2具有氧化性,可用于漂白纸浆
B.CO具有还原性,可用于冶炼铁等金属
C.SiO2熔点高,可用作光导纤维
D.Al2O3具有两性,可用作耐高温材料
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol NaOH的溶液恰好完全反应;另取一份加入含b moI HC1的溶液恰好不再放出气体。则该混合溶液中c(Na+)为
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是 ( )
A.SO2、SiO2、P2O5均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.酒精、冰醋酸、草酸钾均为电解质
D.NH4SCN、SiO2、NH3·H2O均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)求:
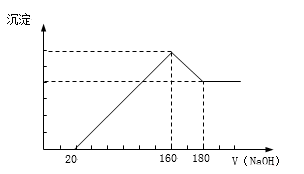
(1)加入NaOH溶液0--20mL过程中反应方程式为:_______________。160--180mL过程中反应方程式为___________________。
(2)合金中Mg的质量为____________g。所用HCl的物质的量浓度为____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O
B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
C.钠与水的反应:Na+H2O=Na++OH-+H2↑
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子最外层上只有两个电子,该元素()
A. 一定是金属元素
B. 一定是ⅡA族元素
C. 一定是过渡元素
D. 可能是金属元素,也可能不是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法不正确的是
A.硅是非金属元素,但它的单质是灰黑色有金属光泽的固体
B.硅的导电性介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质反应
D.当加热到一定温度时,硅能与氧气、氯气等非金属反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 同主族元素自上而下金属性减弱
B. 同主族元素自上而下,得电子能力增强
C. 同周期元素中ⅠA族元素的原子半径最小
D. 同周期元素中ⅦA元素气态氢化物最稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com