
(1)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
科目:高中化学 来源:2014年高二化学人教版选修四 3燃烧热 能源练习卷(解析版) 题型:选择题
已知:
①25 ℃、101 kPa时,2C(s)+O2(g) 2CO(g) ΔH=-221 kJ·mol-1
2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq) H2O(l) ΔH=-57.3 kJ·mol-1
H2O(l) ΔH=-57.3 kJ·mol-1
又已知弱电解质电离吸热。下列结论正确的是( )
A.C的燃烧热大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol 水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 20燃料电池练习卷(解析版) 题型:选择题
质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )
①正极反应为:O2+4H++4e- 2H2O
2H2O
②负极反应为:2H2-4e- 4H+
4H+
③总的化学反应为:2H2+O2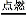 2H2O
2H2O
④氢离子通过电解质向正极移动
A.①②③B.②③④C.①②④D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 19一次电池 二次电池练习卷(解析版) 题型:选择题
纽扣电池可用于计算器、电子表等的电源。有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O+H2O 2Ag+Zn(OH)2。关于该电池的叙述不正确的是( )
2Ag+Zn(OH)2。关于该电池的叙述不正确的是( )

A.使用时电子由Zn极经外电路流向Ag2O极,Zn是负极
B.使用时电子由Ag2O极经外电路流向Zn极,Ag2O是负极
C.正极的电极反应为Ag2O+2e-+H2O 2Ag+2OH-
2Ag+2OH-
D.Zn极发生氧化反应,Ag2O极发生还原反应
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 18原电池练习卷(解析版) 题型:选择题
按下图装置实验,若x轴表示流出负极的电子的物质的量,则y轴应表示( )
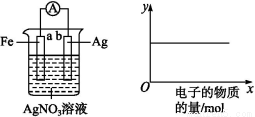
①c(Ag+) ②c(N) ③a棒的质量 ④b棒的质量
⑤溶液的质量
A.①③B.③④C.①②④D.②
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 17难溶电解质的溶解平衡练习卷(解析版) 题型:选择题
某温度下 ,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示,据图分析,下列判断错误的是( )
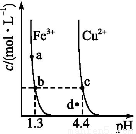
A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B.加适量NH4Cl固体可使溶液由a点变到b点
C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 16盐类水解的应用练习卷(解析版) 题型:选择题
已知0.1 mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 14酸碱中和滴定练习卷(解析版) 题型:填空题
测血钙的含量时,可将2.0 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20.0 mL 1.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 。
(3)计算:血液中含钙离子的浓度为 g·mL-1。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 10化学反应进行的方向练习卷(解析版) 题型:填空题
氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS=-198.2 J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com