
| A. | 将1mL饱和氯化铁溶液逐滴加入到20mL温水中,边加边搅拌 | |
| B. | 向Fe(OH)3胶体中加入少量H2SO4溶液,会生成红褐色沉淀 | |
| C. | 可利用丁达尔效应区分胶体和溶液 | |
| D. | 胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 |
分析 A.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和的氯化铁溶液;
B.硫酸少量胶体发生聚沉;
C.丁达尔效应是胶体特有性质;
D.只有胶粒带有电荷的胶体在通电时发生电泳现象.
解答 解:A.制备氢氧化铁胶体应在沸腾的蒸馏水中加入饱和的氯化铁溶液,故A错误;
B.硫酸少量胶体发生聚沉,所以会产生沉淀,故B正确;
C.丁达尔效应是胶体特有性质,可利用丁达尔效应区分胶体和溶液,故C正确;
D.胶体具有吸附性,吸附阳离子或阴离子,则胶体粒子带电,在电场作用下会产生电泳现象,故D正确;
故选:A.
点评 本题考查了胶体性质的分析应用,主要是胶体特征性质的理解,掌握基础是关键,题目较简单,注意对基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a=b | C. | a<b | D. | 2a=b |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
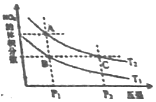 反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是( )| A. | A、C两点的反应速率:A>C | |
| B. | A、C两点的化学平衡常数:A>C | |
| C. | A、C两点N2O4的转化率:A>C | |
| D. | 由状态B到状态A,可以用加热的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 2 mol、2 mol、6 mol | B. | 5 mol、2 mol、6 mol | ||
| C. | 4 mol、2 mol、5 mol | D. | 3 mol、2 mol、6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.050 |
| 4 | 0.050 | 0.025 |
| 5 | 0.040 | |
| 8 | 0.020 |
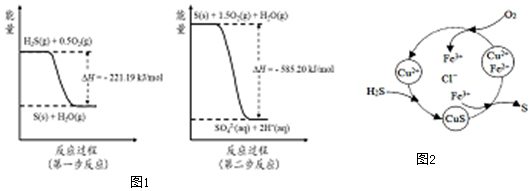
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 向氢氧化铜中滴加稀盐酸:Cu(OH)2+2H+═Cu2++2H2O | |
| D. | 锌粒与稀醋酸反应:Zn+2H+═Zn2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
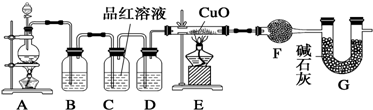
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com