
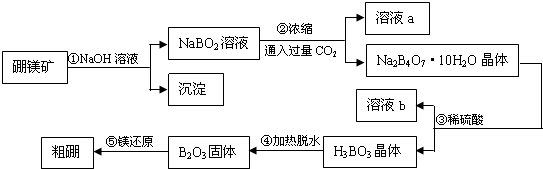
分析 硼镁矿与氢氧化钠溶液反应,过滤除去杂质,NaBO2溶液中,通入过量的二氧化碳,得到Na2B4O7•10H2O与为NaHCO3,过滤分离,由于硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,故Na2B4O7•10H2O晶体与硫酸反应得到硼酸,溶液b中含有硫酸钠,硼酸晶体加热分解得到B2O3,最后用Mg还原得到粗硼.
(1)根据化合价代数和为0计算B元素化合价;
(2)由上述分析可知,第①步通入过量二氧化碳,则a为NaHCO3,第③步加入硫酸,b为Na2SO4;
(3)第①步为Mg2B2O5.H2O与氢氧化钠溶液反应生成NaBO2与Mg(OH)2;
(4)步骤⑤是Mg与B2O3发生置换反应生成B与MgO;
(5)符合复分解反应由强酸制弱酸的原理;
(6)BF3分子中B原子与F原子之间形成1对共用电子对.
解答 解:硼镁矿与氢氧化钠溶液反应,过滤除去杂质,NaBO2溶液中,通入过量的二氧化碳,得到Na2B4O7•10H2O与为NaHCO3,过滤分离,由于硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,故Na2B4O7•10H2O晶体与硫酸反应得到硼酸,溶液b中含有硫酸钠,硼酸晶体加热分解得到B2O3,最后用Mg还原得到粗硼.
(1)根据化合价代数和为0,可知Mg2B2O5•H2O中B的化合价为+3,
故答案为:+3;
(2)由上述分析可知,第①步通入过量二氧化碳,则a为NaHCO3,第③步加入硫酸,b为Na2SO4,
故答案为:NaHCO3;Na2SO4;
(3)第①步为Mg2B2O5.H2O与氢氧化钠溶液反应生成NaBO2与Mg(OH)2,反应方程式为:Mg2B2O5•H2O+2NaOH=2NaBO2+2Mg(OH)2,
故答案为:Mg2B2O5•H2O+2NaOH=2NaBO2+2Mg(OH)2;
(4)步骤⑤是Mg与B2O3发生置换反应生成B与MgO,反应方程式为:B2O3+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$2B+3MgO,
故答案为:B2O3+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$2B+3MgO;
(5)步骤③中化学反应可以发生的原因是:硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,从溶液中析出有利于该反应的进行,
故答案为:强酸制弱酸原理;
(6)BF3分子中B原子与F原子之间形成1对共用电子对,B原子形成3故B-F键,故分子中B原子最外层电子数为3+3=6,F原子最外层电子数为7+1=8,
故答案为:6;8.
点评 本题考查化学制备方案,理解工艺流程原理是解题关键,侧重对化学用语的考查,需要学生具备扎实的基础与灵活运用的能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Z>Y>X | |
| B. | X与R的核电荷数相差18 | |
| C. | 气态氢化物稳定性:W>R | |
| D. | Y与Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 | |
| B. | 对于物质的量浓度相同的氢氧化钠和氨水,加水稀释至m倍和n倍后,若稀释后溶液的pH相等,则m<n | |
| C. | 在中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须经干燥或润洗后方可使用 | |
| D. | 25℃时NH4Cl溶液的Kw大于100℃时NaCl溶液的Kw |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com