
【题目】同温同压下,具有相同体积的任何气体中含有的分子数相同.在一定温度和压强下,10体积气体A2跟30体积气体B2化合生成20体积某气体C,则气体C的化学式为( )
A.AB
B.A2B
C.AB3
D.AB2
科目:高中化学 来源: 题型:
【题目】下列有关化学与科研、生产、生活相关的说法不正确的是( )
A.84消毒液能消杀新冠病毒,它也具有漂白性
B.常用铝槽车装运浓硫酸及浓硝酸是因为它们和铝不发生化学反应
C.锂离子电池是新一代可充电的绿色电池
D.电力是污染最小的一种二次能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某反应aA(g)+bB(g)![]() cC(g)△H="Q" 在密闭容器中进行,在不同温度(T1和T2)及压强(P1和P2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
cC(g)△H="Q" 在密闭容器中进行,在不同温度(T1和T2)及压强(P1和P2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )

A. T1<T2,P1<P2,a+b>c,Q<0
B. T1>T2,P1<P2,a+b<c,Q>0
C. T1<T2,P1>P2,a+b<c,Q>0
D. T1<T2,P1>P2,a+b>c,Q<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为盐酸介质中,金属铜与氢叠氮酸(HN3)构成的原电池,总反应方程式为: 2Cu+2Cl- +HN3+3H+=2CuCl(s)+N2↑+NH4+。下列叙述错误的是
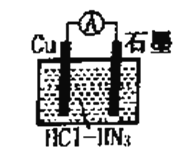
A. 电子的流向为Cu→![]() →石墨
→石墨
B. 负极的电极反应式为Cu+Cl――e-=CuCl(s)
C. 反应一段时间后正极区溶液的pH减小
D. 标准状况下,生成224mL N2时,铜转移的电子数为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热稳定系数和总氯量是漂白粉行业标准里的两个指标。
Ⅰ.利用如图装置(省略加热装置),探究漂白粉的热分解产物。资料显示:久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2。

(1)加热干燥漂白粉样品,观察到B中有大量无色气泡产生。则次氯酸钙分解的固体产物中一定有________。
(2)加热久置于潮湿环境中的漂白粉样品,观察到B中也有气泡产生。
①B中发生反应的离子方程式为_______。
②待充分反应后,断开连接A、B的橡皮管,停止加热,冷却。利用B中产物,通过实验证明加热时有少量氯气生成。请设计实验方案:_________。
Ⅱ. 测定漂白粉总氯的百分含量(即样品中氯元素总质量与样品总质量的比值)。实验步骤如下:
①准确称取5.000 g漂白粉样品,研细,加蒸馏水溶解并冷却后,稀释至500 mL。
②移取25.00 mL该试样溶液至锥形瓶中,调节pH,缓慢加入适量3% H2O2水溶液,搅拌至不再产生气泡。加入适量K2CrO4溶液作为指示剂,以0.1000mol/L AgNO3标准溶液滴定至终点。多次实验,测得消耗AgNO3标准溶液平均体积为25.00 mL。(已知:Ksp(AgCl,白色)=1.56×10-10,Ksp(Ag2Cr2O4,砖红色)=9.0×10-12)
(3)步骤①中,溶解、稀释的过程所用的玻璃仪器有烧杯、玻璃棒、____、 ____。
(4)加入H2O2水溶液,搅拌至不再产生气泡,目的是______(用离子方程式表示)。
(5)滴定终点的现象是_______。
(6)该漂白粉总氯的百分含量为__________。
(7)下列操作导致总氯百分含量测定结果偏高的是______。
A.指示剂K2CrO4的用量过多
B.在滴定终点读取滴定管刻度时,俯视标准液液面
C.滴定前滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨与水的电离相似,存在着微弱的电离:2NH3![]()
![]() +
+![]() 。对该体系的说法中错误的是
。对该体系的说法中错误的是
A. 液氨中含有NH3、![]() 和
和![]() 等微粒
等微粒
B. 一定温度下,液氨中c(![]() )与c(
)与c(![]() )的乘积为一常数
)的乘积为一常数
C. 液氨的电离达到平衡时,c(NH3)=c(![]() )=c(
)=c(![]() )
)
D. 只要不加入其他物质,液氨中c(![]() )总是与c(
)总是与c(![]() )相等
)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验是化学研究的一种重要手段,现有下图所示A-G七种仪器,请根据要求填空。
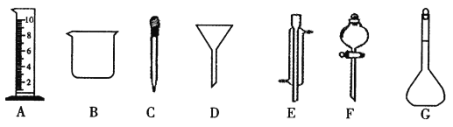
(1)写出仪器名称:E_____________,F_____________。
(2)上述仪器中实验之前需检查装置是否会漏水的是______________(填仪对应字母)。
(3)下列实验操作中用到仪器D的是_________(选填下列选项的编号字母 )。
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
应称取Na2CO3的质量______(g) | 应选用容量瓶的规格 _______(mL) | 除容量瓶外还需要的其它玻璃仪器是上图中的量筒、烧杯、_____(填仪器名称)及玻璃棒 |
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)______________。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作________;配制溶液时,容量瓶未干燥_________;定容时俯视刻度线_________。
(4)在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示各装置的叙述中,正确的是

A. 装置①是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+
B. 装置①中,铁作负极,电极反应式为:Fe3++e-=Fe2+
C. 装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D. 若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com