
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
 ��
������ ��Ԫ�������ڱ���λ�ã���֪��ΪC����ΪN����ΪF����ΪMg����ΪAl����ΪS����ΪCl����ΪAr����ΪK����ΪBr��
��1�����л�ѧ��������õ�Ԫ��ΪAr��ԭ�Ӻ�����18�����ӣ����������Ϊ2��8��8��
��2������Ԫ�غ��ͬ������Ԫ��ԭ���������Ϊԭ�������ϴ��Ԫ���������ں��е�Ԫ��������
��3�����á���������ԭ��Ӧ�У������������Դ����������ԭ������Ʒ�ӦCl2+2NaBr=2NaCl+Br2��
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪC����ΪN����ΪF����ΪMg����ΪAl����ΪS����ΪCl����ΪAr����ΪK����ΪBr��
��1�����л�ѧ��������õ�Ԫ��ΪAr��ԭ�Ӻ�����18�����ӣ����������Ϊ2��8��8��ԭ�ӽṹʾ��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
��2����Ԫ����F����Ԫ����Br��Ϊͬ����Ԫ�أ����ߺ˵����֮��Ϊ8+18=26���ʴ�Ϊ��26��
��3��Ԫ�آ�Ϊ�ȣ�Ԫ�آ�Ϊ�壬�ȵ��ʽ�����������Ϊ�嵥�ʾ���֤���Ȼ����������ǿ������ˮ���뵽�廯����Һ�У������������Ȼ�̼�������Ȼ�̼�����ɫ��֤�������ȱȵ�����������ǿ���ʴ�Ϊ��Cl2+2NaBr=2NaCl+Br2����������ˮ����ʢ���廯����Һ���Թ��У������������Ȼ�̼������������ˮ����Һ�ʻ�ɫ�������������Ȼ�̼�����Ȼ�̼�����ɫ��֤�������ȱȵ�����������ǿ��
���� ����Ԫ�������ɵĿ���һ���Ѷȶ��������ø�������Ŀ�Ĺؼ���Ҫ��ͷ������һ������ȷ��Ԫ�����ڱ�����������ȷ�ж�Ԫ�أ������ش����ص����⣮�������ʵ����Ȼ�����������¿α��Ҫ��


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�� | �����Ϣ |
| T | T�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ������������ |
| X | X��ԭ�����������������ڲ������������ |
| Y | �ڵ�������Ԫ���У�Y�ļ����Ӱ뾶��С |
| Z | T��X��Z��ɵ�36���ӵĻ�����A�Ǽ�������������Ҫ�ɷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ȩ�ܷ���������Ӧ�����ܷ�����ԭ��Ӧ | |
| B�� | ����������ˮ����ȡ����Ӧ | |
| C�� | ������Ӧ�ǿ��淴Ӧ | |
| D�� | �Ҵ������ѻ�Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ̼������ | B�� | �������� | C�� | �������� | D�� | ���ᱵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ�������Ʒ�Ӧ����������CH3CH2OH+Na��CH3CH2ONa+H2�� | |
| B�� | ����Ũ���ᡢŨ����Ļ����Һ��������������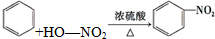 | |
| C�� | �������Ҵ�������Ӧ��������������CH3CH2OH+CH3COOH$��_{��}^{����}$CH3COOCH2CH3 | |
| D�� | ��ϩʹ������Ȼ�̼��Һ��ɫ��CH2=CH2+Br2��CH2BrCH2Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ԭ�������ĵ�����ԭ���������������Ǵ�1��8�ظ����� | |
| B�� | Ԫ�ص���������ԭ�������ĵ������������Ա仯 | |
| C�� | ����ԭ�������ĵ�����Ԫ�ص�������۴�+1��+7�����۴�-7��-1�ظ����� | |
| D�� | Ԫ�������ɵ�ʵ����Ԫ�ػ��ϼ۳������Ա仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ס������缫���ԭ���ʱ�����Ǹ��� | |
| B�� | ͬ��̬�������ӣ��ױ��ҵ�������ǿ | |
| C�� | ����ϡ���ᷴӦ�ų����������������ϡ���ᷴӦ�ų������������ | |
| D�� | ��������ԭ��Ӧ�У���ԭ��ʧȥ�ĵ��ӱ���ԭ��ʧȥ�ĵ��Ӷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com