
| A. | 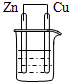 酒精 | B. | 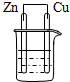 稀H2SO4 | C. | 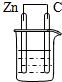 酒精 | D. | 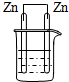 稀H2SO4 |
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 恒温压缩体积,平衡不移动,颜色加深 | |
| B. | 恒容充入H2,I2的百分比含量降低 | |
| C. | 恒容充入HI,开始时正反应速率减小 | |
| D. | 恒容,降低温度正反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高铁酸盐(含FeO42-离子)是新型、高效、多功能水处理剂,既能消毒杀菌又能净水 | |
| B. | 用硫酸清洗锅炉中的水垢 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 使用Na2S作沉淀剂,可有效除去废水中Cu2+和Hg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “氯碱法”的副产品为氢气 | B. | “铝热法”常用于冶炼铁 | ||
| C. | “空气吹出法”用于海水中提取碘 | D. | “侯氏制碱法”制得的是火碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 2NO(g)+2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| D. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
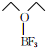 )的熔点为-58℃,沸点为126~129℃,它属于分子晶体.
)的熔点为-58℃,沸点为126~129℃,它属于分子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
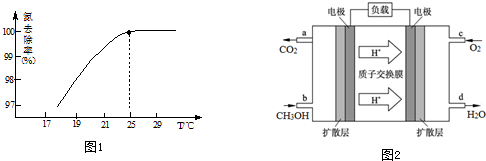
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com