
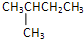 、
、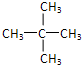 ,
, ,选最长的碳连做主链,主链有3个碳原子,主链为丙烷,在2号C含有2个甲基,该有机物命名为:2,2-二甲基丙烷,
,选最长的碳连做主链,主链有3个碳原子,主链为丙烷,在2号C含有2个甲基,该有机物命名为:2,2-二甲基丙烷, ;2,2-二甲基丙烷;3.
;2,2-二甲基丙烷;3.


科目:高中化学 来源: 题型:
| A、卤代烃在NaOH存在下水解生成的有机物都是醇 |
| B、所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
C、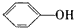 与 与  互为同系物 互为同系物 |
| D、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 相对分 子质量 |
密度 (g?cm-3) |
沸点 ℃ |
溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:

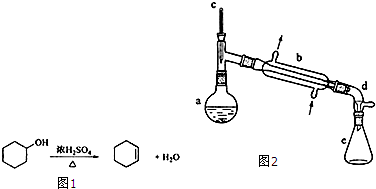
 转变为
转变为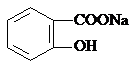 的流程为
的流程为
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 ⑥
⑥ ⑦CH3CHO ⑧HCOOH ⑨
⑦CH3CHO ⑧HCOOH ⑨ ⑩
⑩

查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 1 | 2 | 3 | 4 |
| Na2S2O3溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 20.01 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期表目前共有8个周期 |
| B、元素周期表中共有十八个族,其中有主族、副族、0族和Ⅷ族 |
| C、元素周期表中第一、二、三周期为短周期 |
| D、元素周期表中第IA族全部是金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com