
| A. | 增大反应物浓度 | B. | 升高温度 | C. | 增大压强 | D. | 加入正催化剂 |
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{2b-a}{20}$ | B. | 2b-a | C. | 5b-$\frac{5a}{2}$ | D. | 10b-5a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.请回答下列问题:
一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
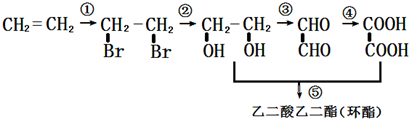
 ;
; +H2O,;
+H2O,; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 压强P1<P2 | B. | a+b<c+d | C. | T1<T2 | D. | △H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al (Fe):浓硝酸 | B. | MgO(Al2O3):盐酸 | ||
| C. | FeCl3(FeCl2):氯水 | D. | FeCl2(CuCl2):氢氧化氢钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com