
| 序号 | 甲 | 乙 | 丙 |
| A | Cl2 | SO2 | Ba(NO3)2 |
| B | HCl | CO2 | 石灰水 |
| C | NH3 | SO2 | Ba(OH)2 |
| D | NO2 | SO2 | BaCl2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氯气和二氧化硫按体积比为1:1,两者恰好完全反应生成硫酸和盐酸,硫酸与硝酸钡反应生成硫酸钡沉淀;
B、氯化氢和二氧化碳的混合气体通入石灰水,首先反应的盐酸,而0.2mol的盐酸与石灰水反应盐酸过量;
C、氨气和二氧化硫的混合气体,通入氢氧化钡生成亚硫酸钡沉淀;
D、二氧化氮与二氧化硫的混合气体通入氯化钡生成硫酸钡沉淀.
解答 解:A、氯气和二氧化硫按体积比为1:1,两者恰好完全反应生成硫酸和盐酸,硫酸与硝酸钡反应生成硫酸钡沉淀,有沉淀产生,故A不选;
B、氯化氢和二氧化碳的混合气体通入石灰水,首先反应的盐酸,而0.2mol的盐酸与石灰水反应盐酸过量,所以无沉淀产生,故B选;
C、氨气和二氧化硫的混合气体,通入氢氧化钡生成亚硫酸钡沉淀,有沉淀产生,故C不选;
D、二氧化氮与二氧化硫的混合气体通入氯化钡生成硫酸钡沉淀,有沉淀产生,故D不选;
故选B.
点评 本题考查元素化合物知识,学生要掌握二氧化碳与氯化氢的混合气体与氢氧化钡反应,首先反应的氯化氢气体和二氧化硫与二氧化氮、氯气发生氧化还原反应,生成硫酸盐,比较容易.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
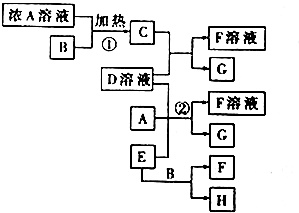
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O | |
| B. | 铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu | |
| C. | 氢氧化铜和硫酸反应 OH-+H+=H2O | |
| D. | 硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
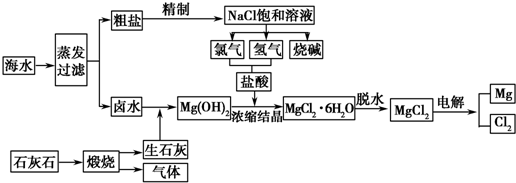
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磺化煤能使具有永久硬度的水软化,因为它能除去水中的Ca2+、Mg2+、SO42-和Cl-等 | |
| B. | 经磺化煤软化处理后,软水中Na+浓度增大 | |
| C. | 磺化煤使硬水软化以及磺化煤的再生,这两种操作可以在同一离子交换柱中同时进行 | |
| D. | 失去软化硬水能力的磺化煤,不可能恢复它的软化能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 5.6 g Fe和足量的氯气完全反应失去电子数为0.3NA | |
| B. | 0.1molNa2O2固体与足量的H2O充分反应,转移0.2NA个电子 | |
| C. | 常温常压下,23 g NO2和N2O4的混合气体一定含有NA个氧原子 | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
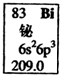
| A. | Bi元素的质量数是209 | |
| B. | Bi原子最外层有5个能量相同的电子 | |
| C. | Bi原子6p亚层有一个未成对电子 | |
| D. | Bi元素的相对原子质量是209.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com