
£¨16·Ö£© £¨1£©½«2mol SO2ºÍ1mol O2·ÅÈë2LĂܱƠÈƯÆ÷ÖĐ·¢ÉúÈçÏ·´Ó¦£º
2SO2+O2 2SO3¡÷H£¼0
2SO3¡÷H£¼0
µ±´ïµ½Æ½ºâʱ£¬ÓÉÓÚ̀ơ¼₫¸Ä±ä¶ø̉ưÆđ·´Ó¦ËٶȺͻ¯Ñ§Æ½ºâµÄ±ä»¯Çé¿ö£¬ÈçÏÂͼ±íʾ£º
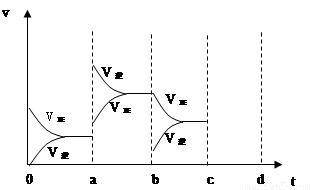
£¨1£©a b¹ư³̀ÖиıäµÄ̀ơ¼₫¿ÉÄÜÊÇ ¡¡¡¡ £»
£¨2£©b c¹ư³̀ÖиıäµÄ̀ơ¼₫¿ÉÄÜÊÇ £»
£¨3£©ÈôÔö´óѹǿʱ£¬·´Ó¦Ëٶȱ仯Çé¿ö»ÔÚc~d´¦£»
(4) ´ïµ½µÚ̉»¸öƽºâʱ£¬²âµĂƽºâʱSO3µÄŨ¶ÈΪ0.5mol/L¡£Çë¼ÆËă´Ë̀ơ¼₫ϵÄƽºâ³£ÊưºÍSO2µÄת»¯ÂÊ¡££¨̉ªÇóĐ´³ö½ầâ¹ư³̀£©
(¹²16·Ö£©
£¨1£©ÉưΣ»¡¡(2)¼ơĐ¡ SO3Ũ¶È£»¡¡
(3) Èçͼ£¨¸÷2·Ö£¬£©
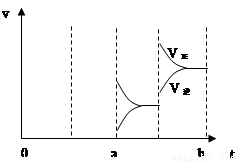
(4) 4£» 50% £¨¹²10·Ö£©
¡¾½âÎö¡¿
ÊỒâ·ÖÎö£º½«2mol SO2ºÍ1mol O2·ÅÈë2LĂܱƠÈƯÆ÷ÖĐ·¢ÉúÈçÏ·´Ó¦£º
2SO2+O2 2SO3¡÷H£¼0
2SO3¡÷H£¼0
a¡ªbµÄ±ä»¯£¬¿É̉Ô¿´µ½£¬ƠưÄæ·´Ó¦ËÙÂʶ¼·¢ÉúÁËͻԾ£¬¶øÇ̉£¬Äæ·´Ó¦ËÙÂÊ´óÓÚƠư·´Ó¦ËÙÂÊ£¬ÓÉÓڸ÷´Ó¦·ÅÈÈ£¬Ëù̉ÔabµÄ̀ơ¼₫¸Ä±äÊÇÉưΣ¬b¡ªcµÄ±ä»¯£¬Äæ·´Ó¦ËÙÂÊͻԾϽµ£¬Ơư·´Ó¦ËÙÂÊÁ¬Đø½µµÍ£¬¸Ä±äµÄ̀ơ¼₫¿ÉÄÜÊǼơĐ¡ SO3Ũ¶È£»
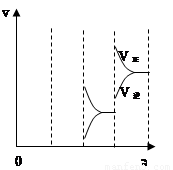
ÈôÔö´óѹǿʱ£¬·´Ó¦Ëٶȱ仯Çé¿öÈçÉÏͼ:
´ïµ½µÚ̉»¸öƽºâʱ£¬²âµĂƽºâʱSO3µÄŨ¶ÈΪ0.5mol/L¡£
2SO2 +
O2  2SO3¡÷H£¼0
2SO3¡÷H£¼0
ÆđʼŨ¶È 1 0.5 0
±ä»¯Å¨¶È 0.5 0.25 0.5
ƽºâŨ¶È 0.5 0.25 0.5
´Ë̀ơ¼₫ϵÄƽºâ³£ÊưK=C2(SO3)/C2(SO2)*C(O2) =4¡£
SO2µÄת»¯ÂÊ=0.5/1=50%¡£
¿¼µă£º»¯Ñ§Æ½ºâ³£Êư ·´Ó¦ËÙÂʵÄÓ°Ị̈́̉ËØ
µăÆÀ£º»¯Ñ§Æ½ºâ³£Êư£¬ÊÇÖ¸ÔÚ̉»¶¨Î¶ÈÏ£¬¿ÉÄæ·´Ó¦Î̃ÂÛ´ÓƠư·´Ó¦¿ªÊ¼£¬»¹ÊÇ´ÓÄæ·´Ó¦¿ªÊ¼£¬̉²²»¹Ü·´Ó¦ÎïÆđʼŨ¶È´óĐ¡£¬×îºó¶¼´ïµ½Æ½ºâ£¬Ơâʱ¸÷Éú³ÉÎïŨ¶ÈµÄ»¯Ñ§¼ÆÁ¿Êư´ÎĂƯµÄ³Ë»ư³ửÔ¸÷·´Ó¦ÎïŨ¶ÈµÄ»¯Ñ§¼ÆÁ¿Êư´ÎĂƯµÄ³Ë»ưËùµĂµÄ±ÈÖµÊǸö³£Êư£¬ÓĂK±íʾ£¬Ơâ¸ö³£Êư½Đ»¯Ñ§Æ½ºâ³£Êư¡£Æ½ºâ³£Êử»°ăÓĐŨ¶Èƽºâ³£ÊưºÍѹǿƽºâ³£Êư¡£
ÔÚÊéĐ´Æ½ºâ³£Êư±í´ïʽʱ£¬̉ª×¢̉ẩÔÏÂÎỀ⣺
¢Ù ÔÚÓ¦ÓĂƽºâ³£Êư±í´ïʽʱ£¬Ï¡ÈÜ̉ºÖеÄË®·Ö×ÓŨ¶È¿É²»Đ´¡£̣̉ΪϡÈÜ̉ºµÄĂܶȽӽüÓÚ1 g/mL¡£Ë®µÄÎïÖʵÄÁ¿Å¨¶ÈΪ55.6 mol/L¡£ÔÚ»¯Ñ§±ä»¯¹ư³̀ÖĐ£¬Ë®Á¿µÄ¸Ä±ä¶ÔË®µÄŨ¶È±ä»¯Ó°Ḯ¼«Đ¡£¬Ëù̉ÔË®µÄŨ¶ÈÊÇ̉»¸ö³£Êư£¬´Ë³£Êư¿É¹é²¢µ½Æ½ºâ³£ÊưÖĐÈ¥¡£
¶ÔÓÚ·ÇË®ÈÜ̉ºÖеķ´Ó¦£¬ÈܼÁµÄŨ¶ÈͬÑùÊdz£Êư¡£
¢Ú µ±·´Ó¦ÖĐÓĐ¹̀̀åÎïÖʲμÓʱ£¬·Ö×Ó¼äµÄÅöײֻÄÜÔÚ¹̀̀å±íĂæ½øĐĐ£¬¹̀̀åµÄÎïÖʵÄÁ¿Å¨¶È¶Ô·´Ó¦ËÙÂʺÍƽºâĂ»ÓĐÓ°Ḯ£¬̣̉´Ë£¬¹̀̀åµÄ¡°Å¨¶È¡±×÷Ϊ³£Êư£¬ÔÚƽºâ³£Êư±í´ïʽÖĐ£¬¾Í²»Đ´¹̀̀åµÄŨ¶È¡£
¢Û »¯Ñ§Æ½ºâ³£Êư±í´ïʽÓ뻯ѧ·½³̀ʽµÄÊéĐ´·½Ê½ÓĐ¹Ø¡£Í¬̉»¸ö»¯Ñ§·´Ó¦£¬ÓÉÓÚÊéĐ´µÄ·½Ê½²»Í¬£¬¸÷·´Ó¦Îï¡¢Éú³ÉÎïµÄ»¯Ñ§¼ÆÁ¿Êư²»Í¬£¬Æ½ºâ³£Êư¾Í²»Í¬¡£µ«ÊÇƠâĐ©Æ½ºâ³£Êư¿É̉ÔÏ໥»»Ëă¡£
¢Ü ²»Í¬µÄ»¯Ñ§Æ½ºầåϵ£¬Æäƽºâ³£Êư²»̉»Ñù¡£Æ½ºâ³£Êư´ó£¬ËµĂ÷Éú³ÉÎïµÄƽºâŨ¶È½Ï´ó£¬·´Ó¦ÎïµÄƽºâŨ¶ÈÏà¶Ô½ÏĐ¡£¬¼´±íĂ÷·´Ó¦½øĐĐµĂ½ÏÍêÈ«¡£̣̉´Ë£¬Æ½ºâ³£ÊưµÄ´óĐ¡¿É̉Ô±íʾ·´Ó¦½øĐĐµÄ³̀¶È¡£
¢Ử»°ăÈÏΪK>10^5·´Ó¦½ÏÍêÈ«£¨¼´²»¿ÉÄæ·´Ó¦£©£¬K<10^(-5)·´Ó¦ºÜÄѽøĐĐ£¨¼´²»·´Ó¦£©¡£
ƽºâ³£ÊưµÄÊưÖµ´óĐ¡¿É̉ÔÅĐ¶Ï·´Ó¦½øĐĐµÄ³̀¶È¡£


 Ó¢²Åµă½̣ϵÁĐ´đ°¸
Ó¢²Åµă½̣ϵÁĐ´đ°¸ º́¹û×ÓÈư¼¶²âÊÔ¾íϵÁĐ´đ°¸
º́¹û×ÓÈư¼¶²âÊÔ¾íϵÁĐ´đ°¸ ¿Î̀ĂÁ·¼Ó²âϵÁĐ´đ°¸
¿Î̀ĂÁ·¼Ó²âϵÁĐ´đ°¸
| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
| 6 |
| 7 |
| 6 |
| 7 |
| 20 |
| 7 |
| 20 |
| 7 |
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
 ̉ÑÖªÔÚ25¡ăC¡¢1.013¡Á105PaÏ£¬1molÇâÆøÍêȫȼÉƠÉú³É̉º̀¬Ë®·Å³ö285kJµÄÈÈÁ¿£¬Çë»Ø´đÏÂÁĐÎỀ⣺
̉ÑÖªÔÚ25¡ăC¡¢1.013¡Á105PaÏ£¬1molÇâÆøÍêȫȼÉƠÉú³É̉º̀¬Ë®·Å³ö285kJµÄÈÈÁ¿£¬Çë»Ø´đÏÂÁĐÎỀ⣺²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
³£ÎÂÏ£¬¿É·¢Éú·´Ó¦£ºA£¨g£©+B£¨g£©?C£¨g£©+xD£¨g£© Èô½«2mol AºÍ2mol B »́ºÏ³äÈë̀å»ư¿É±äµÄĂܱƠÈƯÆ÷ÖĐ£¬ÔÚ²»Í¬Ñ¹Ç¿Ï´ﵽƽºâʱ£¬CµÄŨ¶ÈÈçÏ£º
|
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º2012-2013ѧÄê¹ă¶«¶«Ư¸µÚÆ߸߼¶ÖĐѧ¸ß¶₫ÉÏÆÚÖĐ¿¼ÊÔ»¯Ñ§ÊÔ¾í£¨´ø½âÎö£© ̀âĐÍ£º¼ÆËằâ
£¨16·Ö£© £¨1£©½«2mol SO2ºÍ1mol O2·ÅÈë2LĂܱƠÈƯÆ÷ÖĐ·¢ÉúÈçÏ·´Ó¦£º
2SO2+O2 2SO3¡÷H£¼0
2SO3¡÷H£¼0
µ±´ïµ½Æ½ºâʱ£¬ÓÉÓÚ̀ơ¼₫¸Ä±ä¶ø̉ưÆđ·´Ó¦ËٶȺͻ¯Ñ§Æ½ºâµÄ±ä»¯Çé¿ö£¬ÈçÏÂͼ±íʾ£º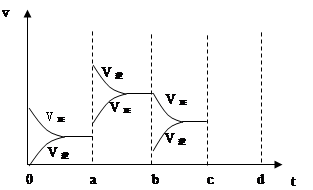
£¨1£©a b¹ư³̀ÖиıäµÄ̀ơ¼₫¿ÉÄÜÊÇ ¡¡¡¡ £»
£¨2£©b c¹ư³̀ÖиıäµÄ̀ơ¼₫¿ÉÄÜÊÇ £»
£¨3£©ÈôÔö´óѹǿʱ£¬·´Ó¦Ëٶȱ仯Çé¿ö»ÔÚc~d´¦£»
(4) ´ïµ½µÚ̉»¸öƽºâʱ£¬²âµĂƽºâʱSO3µÄŨ¶ÈΪ0.5mol/L¡£Çë¼ÆËă´Ë̀ơ¼₫ϵÄƽºâ³£ÊưºÍSO2µÄת»¯ÂÊ¡££¨̉ªÇóĐ´³ö½ầâ¹ư³̀£©
²é¿´´đ°¸ºÍ½âÎö>>
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com