
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
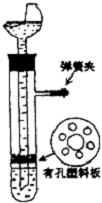 用如图的装置制取氢气,在塑料隔板上放粗锌,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则硫酸由漏斗流下,试管中液面上升与锌粒接触,发生反应,产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止.需要时再打开弹簧夹,又可以使氢气发生.这是一种适用于室温下随制随停的气体发生装置.
用如图的装置制取氢气,在塑料隔板上放粗锌,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则硫酸由漏斗流下,试管中液面上升与锌粒接触,发生反应,产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止.需要时再打开弹簧夹,又可以使氢气发生.这是一种适用于室温下随制随停的气体发生装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化镁粉 | B、氢氧化镁 |
| C、氧化钙 | D、纯碳酸钙粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶液加热 |
| B、小苏打溶液中加入少量NaCl固体 |
| C、氨水中加入少量NH4Cl固体 |
| D、Na2CO3溶液加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K2O |
| B、KO2 |
| C、K2O和K2O2 |
| D、K2O和KO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都易发生取代反应 |
| B、都易发生加成反应 |
| C、乙烯和乙炔易发生加成反应,苯只有在特殊条件下才发生加成反应 |
| D、乙烯和乙炔易被氧化剂氧化,苯不易被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.216g |
| B、0.108g |
| C、0.064g |
| D、0.032g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com