
Ⅰ.CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl·2H2O制备CuCl,并进行相关探究。

【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是 ;
(2)实验操作的先后顺序是 →e(填操作的编号)。
→e(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
【探究反思】
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
Ⅱ.某试液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如下实验:

(1)根据实验现象判断,滤液X中大量存在的阳离子有 ;
(2)沉淀A的化学式 ;沉淀B的化学式 ;
(3)沉淀C的成分 (填“能”或“不能”)确定。若能确定,写出化学式 ;若不能,说明理由 。
(4)该溶液中一定存在的离子是 ;一定不存在的离子是 。
科目:高中化学 来源:2015-2016学年吉林省高二下期末化学试卷(解析版) 题型:选择题
将0.195 g锌粉加入到200 mL的0.100 mol·L-1 MO2+ 溶液中,恰好完全反应,则还原产物可能是 ( )
A.M B.M2+ C.M3+ D.MO2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆哈密二中高二下期末化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+
B.将Fe3O4固体溶于HI溶液中: Fe3O4 + 8H+ = 2Fe3+ + Fe2+ + 4H2O
C.将氯气溶于水:Cl2+H2O═2H++Cl﹣+ClO﹣
D.向FeBr2溶液中通入少量的氯气:2Br-+Cl2 = 2Cl-+Br2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆哈密二中高二下期末化学试卷(解析版) 题型:选择题
下列实验操作或记录正确的是( )
A. 常温常压下测得1 mol N2的质量为28 g
B. 用量筒测得排水法收集制得的氢气体积为50. 28 mL
C. 用两只250 mL的容量瓶配制0.1 mol·L-1500 mL的NaOH溶液ZXXK]
D. 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷(解析版) 题型:选择题
向只含有Fe3+、Cu2+、H+各0.1 mol及a mol SO42-的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是( )
A.当消耗0.1 mol Zn时,得到的还原产物为0.1 mol
B.反应结束时,可得到0.3 mol ZnSO4
C.当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+
D.最后得到的金属单质为Cu
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A. 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
B. 纳米铁粉可以高效地去除被污染水体的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
C. 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线
D. Ba2+浓度较高时危害健康,但BaSO4可服入体内,做为造影剂用于X-射线检查肠胃道疾病
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:填空题
X、Y、Z、W、R是短周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | 原子核内无中子 |
Y | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
Z | 地壳中含量最高的元素 |
W | 原子质量数为23,中子数为12 |
R | 其离子是第三周期金属元素的离子中半径最小的 |
(1)Y、Z、W、R四种元素的原子半径从大到小的顺序是_____________(用元素符号表示)。
(2)Y2电子式为 ;X、Y、Z形成的化合物可用作化肥,该物质所含化学键的类型是 (填共价或离子);X与Z形成的18e-微粒的结构式为 。
(3)砷(As)是人体必需的微量元素,与Y同一主族,A s原子比Y原子多两个电子层,则砷的原子序数为________,
s原子比Y原子多两个电子层,则砷的原子序数为________, 其最高价氧化物的化学式为____________。该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是__________________(用化学式表示)。
其最高价氧化物的化学式为____________。该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是__________________(用化学式表示)。
(4)W在元素周期表中的位置为_______;能够说明W和R金属性强弱的依据有 。
a.W单质的熔点比R单质的熔点低
b.W的化合价比R 的低
的低
c.常温下W单质与水的反应很剧烈,而R单质在加热条件下与水反应现象不明显
d.W最高价氧化物的水化物的碱性比R强
(5)写出工业上冶炼R的化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下期末化学试卷(解析版) 题型:选择题
下列有机物的命名正确的是( )
A.二溴乙烷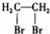
B.3﹣乙基﹣1﹣丁烯 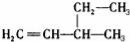
C.2﹣甲基﹣2,4﹣己二烯 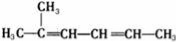
D.2,4,4﹣三甲基戊烷 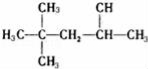
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com