
| A. | 它是高分子化合物 | |
| B. | 它在一定条件下能水解,最终生成葡萄糖 | |
| C. | 是天然蛋白质,仅由C、H、O、N四种元素组成 | |
| D. | 是一种特殊的蛋白质,滴加浓HNO3不发生颜色反应,灼烧时没有任何气味 |
分析 A.高分子化合物是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化合物,多为高聚物;
B.蛋白质是由氨基酸组成的;
C.蛋白质的组成元素主要为:C、H、O、N;
D.蛋白质灼烧有烧焦羽毛气味.
解答 解:A.蛋白质相对分子质量较大,是高分子化合物,故A正确;
B.蛋白质在人体中最终水解为氨基酸,故B错误;
C.蛋白质属于天然高分子化合物,组成元素主要为:C、H、O、N,一般可能还会含有S、P、Fe等元素,故C错误;
D.蛋白质灼烧有烧焦羽毛气味,滴加浓HNO3发生颜色反应变黄色,故D错误.
故选A.
点评 本题考查蛋白质的结构和性质特点,涉及蛋白质的组成元素、水解等知识,难度不大.


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:选择题
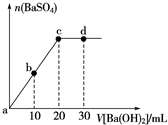
| A. | 溶液的pH:a<b<c<d | B. | 溶液的导电性:c<d | ||
| C. | a、b溶液呈酸性 | D. | c、d溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 CsCl CBr4 CF4 | B. | SiO2 CsCl CF4 CBr4 | ||
| C. | CsCl SiO2 CBr4 CF4 | D. | CF4 CBr4 CsCl SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有氯化铝和氯化镁的混合溶液,向其中滴加a mL 3mol•L-1 NaOH溶液之后,改成滴加cmol/L HCl溶液,所得沉淀的物质的量y(mol)与试剂总体积V(mL)间的关系如图所示.请回答下列问题:
有氯化铝和氯化镁的混合溶液,向其中滴加a mL 3mol•L-1 NaOH溶液之后,改成滴加cmol/L HCl溶液,所得沉淀的物质的量y(mol)与试剂总体积V(mL)间的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、 .
. .
. 、
、 .
. 、
、
 ,如果要合成
,如果要合成 所用的原始原料可以是AC
所用的原始原料可以是AC查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com