
 X ,甲 + 丁
X ,甲 + 丁 Y,丙 + 乙
Y,丙 + 乙 Z ,丁 + 乙
Z ,丁 + 乙 W
W  X :___________________
X :___________________ Y:___________________
Y:___________________ Z :___________________
Z :___________________ W:___________________
W:___________________ 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
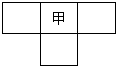 甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如右图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如右图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )| A、元素甲的简单气态氢化物稳定性比乙的强 | B、元素乙在周期表中的位置为第2周期,VIA族 | C、元素丙和元素丁的最高价氧化物对应的水化物均为强酸 | D、4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲(g)的能量一定大于丙(g)的能量 | B、该反应不需要加热 | C、1 mol甲(g)与2 mol乙(g)的总能量高于1 mol丙(g)和1 mol丁(g)的总能量 | D、该反应表示:1 mol甲(g)与2 mol乙(g)在一定条件下反应放出的热量为a kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如右图所示(原子序数:乙>丙)。丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24。下列判断正确的是
|
|
甲 |
|
|
|
|
|
A.元素甲的简单气态氢化物稳定性比乙的强
B.元素乙在周期表中的位置为第2周期,VIA族
C.元素丙和元素丁的最高价氧化物对应的水化物均为强酸
D.4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省泰州市高三上学期期末考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙)。丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24。下列判断正确的是
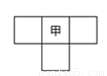
A.元素甲的简单气态氢化物稳定性比乙的强
B.元素丁在周期表中的位置为第3周期,VIA族
C.元素丙和元素丁的最高价氧化物对应的水化物均为强酸
D.4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com