
下列有关判断正确的是( )
A.0.1 mol·L-1Na2SO3溶液中有c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3)
B.0.1 mol·L-1NH4Fe(SO4)2溶液中离子浓度大小关系为c(SO42-)>c(Fe3+)=c(NH4+)>c(H+)>c(OH-)
C.0.2 mol·L-1Na2CO3溶液与0.1 mol·L-1NaHCO3溶液等体积混合后有c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.0.2 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合得到的溶液一定呈酸性
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:2014年高考化学指导冲关 第15练有机化合物的推断与合成练习卷(解析版) 题型:填空题
某烃A是乙烯的同系物,A与乙烯一样,都是重要的化工原料。已知A对氢气的相对密度为21,由A经下列反应可得到G、H两种高分子化合物,它们都是常用的塑料。

请回答下列问题:
(1)E不能使溴的四氯化碳溶液褪色,E的结构简式为______________________;
(2)由A生成B和H的反应方程式分别为___________________________
(3)一定条件下,2 mol F之间脱去1 mol水生成一种具有芳香气味的物质I,写出反应的化学方程式____________________________________________
(4)F的一种同分异构体中有五种不同化学环境的氢原子且能发生银镜反应,写出其结构简式_______________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第11练化学实验基础知识练习卷(解析版) 题型:选择题
实验是化学研究的基础,关于下列各实验装置图的叙述中正确的是( )
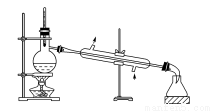
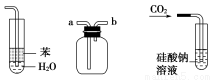
① ② ③ ④
A.装置①:常用于分离互不相溶的液体混合物
B.装置②:可用于吸收NO2或HCl气体,并防止倒吸
C.装置③:先从b口进气集满二氧化碳,再从a口进气,可收集一氧化氮
D.装置④:可用来证明碳的非金属性比硅强
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第10练常见有机化合物及其应用练习卷(解析版) 题型:选择题
下列关于有机物的说法,正确的是( )
A.棉线和蚕丝都能水解生成葡萄糖
B.CH3CH2CH2CH3和CH3CH(CH3)2互为同分异构体
C.1 mol 甲烷和1 mol 氯气在光照条件下充分反应,生成1 mol CH3Cl
D.乙酸乙酯中含有的杂质乙酸可用NaOH溶液除去
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(二) (解析版) 题型:填空题
汽车作为一种现代交通工具正在进入千家万户,汽车尾气的污染问题也成为当今社会急需解决的问题。为使汽车尾气达标排放,催化剂及载体的选择和改良是关键。目前我国研制的稀土催化剂催化转化汽车尾气示意图如图甲:
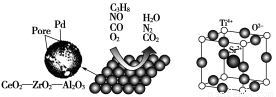
甲 乙
(1)下列有关说法正确的是________。
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、N2都是非极性分子
C.每个N2中,含有2个π键
D.CO的一种等电子体为NO+,它的电子式为[:N??O:]+
(2)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍为0价,镍原子在基态时,核外电子排布式为_____________________;[Ni(CO)4]的配体是________,配位原子是________。
(3)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是________。
(4)为了节省贵重金属并降低成本,也常用钙钛矿型复合氧化物催化剂。一种复合氧化物晶体结构如图乙,则与每个Sr2+紧邻的O2-有________个。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(二) (解析版) 题型:选择题
下列属于取代反应的是( )
①CH3CH=CH2+Br2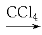 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH+3O2 2CO2+3H2O
2CO2+3H2O
③CH3COOH+CH3CH2OH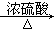 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3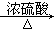 C6H5NO2+H2O
C6H5NO2+H2O
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(三) (解析版) 题型:填空题
二氧化锰可用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
(1)二氧化锰在酸性介质中是一种强氧化剂,请用化学方程式证明:______________________。
(2)锌—锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。
①电池工作时,MnO2发生________反应。
②电池的正极反应式为________。
(3)工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
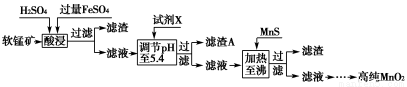
已知:软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物,部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表。
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 |
沉淀物 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
pH | 8.0 | -0.42 | 2.5 | 7 | 7 |
回答下列问题:
①硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为________________________。
②试剂X为________。
③滤渣A的主要成分为________。
④加入MnS的目的主要是除去溶液中的________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习指导预测押题练习卷(一) (解析版) 题型:选择题
下列叙述正确的是( )
A.Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理不相同
C.将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀
D.过量的铜与浓硝酸反应,生成的气体只有NO2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学二轮复习专题滚动练2 化学基本理论练习卷(解析版) 题型:选择题
下列有关化学实验操作合理的是( )
①在配制FeSO4溶液时常向其中加入一定量铁粉和稀硫酸
②配制100 mL 1.00 mol/L的NaCl溶液时,可用托盘天平称取5.85 g NaCl固体
③物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行
④用试管夹从试管底由下往上夹住距试管口约1/3处,手持试管夹长柄末端,进行加热
⑤不慎将浓硫酸沾在皮肤上,立即用NaHCO3溶液冲洗
⑥用广泛pH试纸测得某溶液的pH=12.3
⑦用碱式滴定管量取20.00 mL 0.100 0 mol/L KMnO4溶液
⑧将铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
A.④⑤⑥⑦ B.①④⑤⑦ C.②③⑥⑧ D.①③④⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com