
(1)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时,CO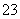 移向电池的 (填“正”或“负”)极。
移向电池的 (填“正”或“负”)极。
 (2)现用氢氧燃料电池进行下图所示实验:
(2)现用氢氧燃料电池进行下图所示实验:
①请写出氢氧燃料电池中的电极反应式:
负极: 正极:
②右图装置中,某一铜电极的质量减轻了3.2 g,则a极上消耗的O2在标准状况下体积为 L。
科目:高中化学 来源: 题型:
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是

A.②、⑧、⑨对应简单离子半径依次减小
B.⑥的氯化物的熔点比⑦的氯化物熔点低
C.元素⑩处于常见周期表第四周期第VIIIB族
D.①分别与③、④、⑤均可形成既含极性键又含非极性键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气分子的空间构型为三角锥形,而甲烷则是正四面体形,这是因为( )
A.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
D.氨气分子是极性分子而甲烷是非极性分子。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个固定容积的密闭容器中,加入mmol A、nmol B,发生下列反应:
mA(g)+nB(g) pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入amol A、bmol B、cmol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )
pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入amol A、bmol B、cmol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )
A、a︰b︰c=m︰n︰p B、a︰b=m︰n (ap/m)+c=p
C、(mc/p)+a=m,(nc/p)+b=n D、a=m/3,b=n/3,c=2p/3
查看答案和解析>>
科目:高中化学 来源: 题型:
在HF、H2O、NH3、CH4、CO32-、CO2、HI分子中
(1)以极性键相结合,具有正四面体结构的非极性分子是 。
(2)以极性键相结合,具有三角锥型结构的极性分子是 。
(3)以极性键相结合,具有V型结构的极性分子是 。
(4)以极性键相结合,而且分子极性最大的是 。
(5)CO32-的空间构型为
查看答案和解析>>
科目:高中化学 来源: 题型:
控制变量法是研究化学变化规侓的重要思想方法。请仔细观察
下表中50 mL稀盐酸和
1g碳酸钙反应的实验数据:
| 实验 序号 | 碳酸钙 状态 | c(HCl) /mol·L-1 | 溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒状 | 0.6 | 20 | 41 | 280 |
| 4 | 粒状 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒状 | 1.0 | 20 | 40 | 120 |
| 7 | 粒状 | 1.0 | 30 | 50 | 40 |
| 8 | 粒状 | 1.2 | 20 | 40 | 90 |
| 9 | 粒状 | 1.2 | 25 | 45 | 40 |
分析并回答下列问题:
(1)本反应属于________反应(填“吸热”或“放热”),反应的离子方程式为 。
(2)实验6和7表明,_________对反应速率有影响,_________反应速率越快,能表明同一规律的实验还有_________(填实验序号)。
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是 。
(4)本实验中影响反应速率的其它因素还有__________,能表明这一规律的实验序号是1、2与_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1 NA
B.100ml 18.4mol/L的浓硫酸与足量铜加热充分反应后生成SO2的数目为0.92 NA
C.密闭容器中盛有0.1molN2和0.3molH2,充分反应后转移电子的数目为0.6NA
D.80 g NH4NO 3晶体中含有NH4+ 数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com