
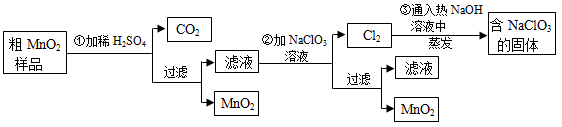


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������Һ��̼��أ���������������Һ |
| B���Ȼ�����Һ���Ȼ�þ��������������������Һ |
| C���Ȼ��ع��壨�������裩������������������Һ |
| D������(�Ȼ�������)���������ı���ʳ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | A | B | C | D |
| ���� | FeCl2(FeCl3) | CO2��CO�� | Fe��A1�� | SiO2��CaCO3�� |
| �����Լ� | Fe | O2 | ������Һ | �������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| �ζ����� | ������Һ�����/mL | ����Һ����� | |
| �ζ�ǰ�̶�/mL | �ζ���̶�/mL | ||
| 1 | 25.00 | 1.02 | 21.04 |
| 2 | 25.00 | 2.00 | 22.00 |
| 3 | 25.00 | 0.20 | 20.21 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
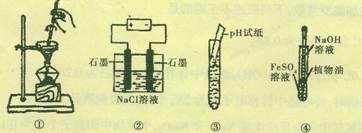
| A��ͼ�ٱ�ʾ�ӵ�ˮ�з������IJ������� |
| B��ͼ��Ϊ����Ȼ�����Һ��װ�ã�һ��ʱ��������ռ�����������֮��һ��Ϊ1:1 |
| C��ͼ��Ϊ�ⶨ��ҺpH��ʵ����� |
| D��ͼ�ܿ��������Ʊ��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
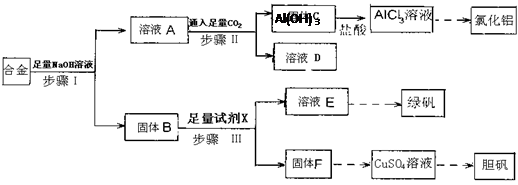
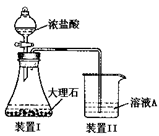
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����еļױ����ữ���������Һ ��Һ�� | B���Ҵ��е�ˮ����ˮ����ͭ ��� |
| C���Ҵ��е����ᣨNaOH��Һ ��Һ�� | D���������е��Ҵ� ��(ˮ ��Һ) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 _____________________��
_____________________���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com