
对于恒容密闭容器中发生的可逆反应N2(g)+3H2(g)  2NH3(g) ΔH<0,能说明反应达到化学平衡状态的是( )
2NH3(g) ΔH<0,能说明反应达到化学平衡状态的是( )
A.断开1个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.N2、H2、NH3分子数之比为1:3:2
科目:高中化学 来源: 题型:
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(杂质中不含铁元素,且杂质不与H2、H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
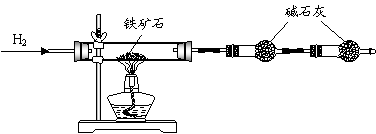 Ⅰ.铁矿石中含氧量的测定
Ⅰ.铁矿石中含氧量的测定
|
实验结果:将5.0g铁矿石放入硬质玻璃管中完全反应, 测得装置B增重1.35 g。
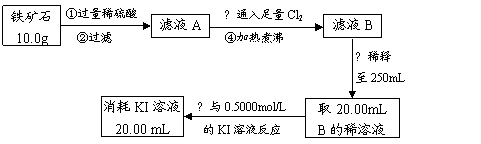 Ⅱ.铁矿石中含铁量的测定
Ⅱ.铁矿石中含铁量的测定
Ⅲ.问题讨论与解决:
(1)如要验证滤液A中铁元素的存在形式,可另取两份滤液A分别进行实验,实验方法、现象与结论如下表。请将其补充完整。
可供选择的试剂有:酸性KMnO4溶液、NaOH溶液、KSCN溶液、氯水
| 实验方法 | 实验现象 | 结论 |
| 步骤1:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe3+ |
| 步骤2:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe2+ |
(2)步骤④中煮沸的作用是: ▲ ;
(3)步骤③中反应的离子方程式为: ▲ ;
(4)请通过实验Ⅰ、Ⅱ计算出该铁矿石中铁的氧化物的化学式。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_______________;
(2)反应开始至2 min,气体Z的反应速率为____________;
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________倍;
②若此时将容器的体积缩小为原来的 0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下现象与电化腐蚀无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 B.生铁比软铁芯(纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处易生铁锈 D.银质奖牌久置后表面变暗
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应xA(g)+yB(g) zC(g)中,物质的含量R%(A%和C%)随温度的变化曲线如图所示,下列说法正确的是
zC(g)中,物质的含量R%(A%和C%)随温度的变化曲线如图所示,下列说法正确的是
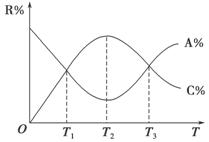
A.T3温度对应的化学反应速率低于T2温度对应的化学反应速率
B.该反应在T2温度时达到了化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
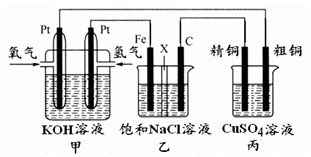
根据要求回答相关问题:
(1)通入氢气的电极为 (填“正极”或“负极”),负极的电极反应式为 。
(2)石墨电极为 (填“阳极”或“阴极”), 乙装置中阳极的电极反应式为_____________。
(3)反应一段时间后,在乙装置中滴入酚酞溶液, _ 区(填“铁极”或“石墨极”)的溶液先变红。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 (填“增大”“减
小”或“不变”)。
(5)若在标准状况下,有224m L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为 ;丙装置中阴极析出铜的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
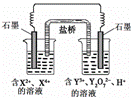
右下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
A.左池电极反应式:X4+ + 2e-=X2+
B.每消耗1mol Y2O72-,转移3mol电子
C.改变右池溶液的c(H+),电流强度不变
D.左池中阴离子数目增加
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示正确的是
A.质子数为35、中子数为45的溴原子: Br
Br
B.过氧化钠的电子式:
C.硫离子的结构示意图:

D.苯的结构简式:C6H6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com