
下列影响化学反应速率的因素中,是通过改变活化分子百分数来实现的是
①改变气体物质的浓度 ②改变气体的压强
③加入催化剂 ④改变气体的温度
A.只有①② B.只有③④ C.只有①③④ D.①②③④
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:选择题
室温下向10mL0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )

A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A—)+c(HA)
D.b点所示溶液中c(A—)>c(HA)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上第一次学段考试化学卷(解析版) 题型:选择题
由CO和CO2组成的混合气体,密度是相同条件下氢气密度的18倍,则该混合气体中CO和CO2的体积比为 ( )
A.1:1 B.1:2 C.2:1 D.2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上第一次月考化学试卷(解析版) 题型:填空题
(1)在101 kPa时,足量H2在1 mol O2中完全燃烧生成2 mol液态水,放出571.6 kJ的热量,H2的燃烧热△H= ,表示H2燃烧热的热化学方程式为 。
(2)1.00 L 1.00 mol·L-1硫酸与2.00 L 1.00 mol·L-1 NaOH溶液完全反应,放出114.6 kJ的热量,该反应的中和热△H= ,表示其中和热的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上第一次月考化学试卷(解析版) 题型:选择题
某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=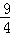 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
A. 平衡时,乙中CO2的转化率大于60%
B. 平衡时,甲中和丙中H2的转化率均是60%
C. 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市如东县徐州市丰县高三10月联考化学卷(解析版) 题型:实验题
茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如图操作:

请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
离子 | Ca2+ | Fe3+ |
完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的 。
(2)写出从滤液A→沉淀D的离子反应方程式 。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,判断D已经沉淀完全方法是 。
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O。
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L﹣1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.

A B C D
图1 图2
① 此步操作过程中KMnO4标准溶液应装在图2中哪个仪器中(填写字母) 。
②滴定到终点,现象 ,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将 (填“偏高”“偏低”或“无影响”)。
(5)原茶叶中钙元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市如东县徐州市丰县高三10月联考化学卷(解析版) 题型:选择题
已知漂白液是含有NaClO和NaCl混合溶液(pH>7),下列关于该溶液说法正确的是
A.该溶液中,Ag+、K+、NO3?、Mg2+可以大量共存
B.该溶液中,H+、NH4+、SO42?、I? 可以大量共存
C.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023
D.向该溶液中滴入少量Na2SO3溶液,反应的离子方程式为:SO32?+ClO? == Cl?+ SO42?
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三联合考试化学试卷(解析版) 题型:实验题
三氯化硼的熔点为-107.3℃,沸点为12.5℃,易水解生成硼酸和氯化氢,可用于制造高纯硼、有机合成催化剂等。实验室制取三氯化硼的原理为:B2O3+3C+3Cl2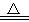 2BCl3+3CO
2BCl3+3CO
(1)甲组同学拟用下列装置制取纯净干燥的氯气(不用收集)。
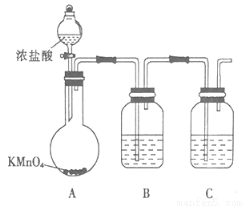
①装置B中盛放的试剂是 ,装置C的作用是 。
②装置A中发生反应的离子方程式为 。
(2)乙组同学选用甲组实验中的装置A、B、C和下列装置(装置可重复使用)制取BCl3并验证反应中有CO生成。

①乙组同学的实验装置中,依次连接的合理顺序为
A→B→C→ → → → → →F→D→I。
②实验开始时,先通入干燥N2的目的是 。
③能证明反应中有CO生成的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com