
【题目】常温下,向某溶液中加水稀释时,c(OH-)/c(H+)的值明显增大,在该溶液中能大量共存的离子组是( )
①Al3+、Na+、NO![]() 、AlO
、AlO![]() ②K+、Fe2+、I-、SO
②K+、Fe2+、I-、SO![]()
③Ba2+、I-、NO![]() 、Na+ ④Na+、Ca2+、Mg2+、Cl-
、Na+ ④Na+、Ca2+、Mg2+、Cl-
A. ①② B. ①③ C. ②④ D. ②③
科目:高中化学 来源: 题型:
【题目】汽车尾气中通常含有NO和CO等大气污染物,科学家寻找高效催化剂实现了汽车尾气的转化,进而减少汽车尾气对大气的污染。
(1)在100 kPa和298.15 K下,由稳定单质生成1 mol化合物的焓变称为该物质在 298.15 K时的标准摩尔生成焓。已知NO标准摩尔生成焓AH= +91.5 kJ/moI,CO的标准燃烧热AH=- 283kJ/mol,由此写出NO和CO反应的热化学反应方程式____。
(2) 一定温度下,向2L恒容密闭容器中充入4.0molNO2和4.0molCO,在催化剂作用下发生反应4CO(g)+2NO2(g) = N2(g)+4CO2(g) △H<0,测得相关数据如下:

①5~l0min,用NO2的浓度变化表示的反应速率为____。
②以下表述能说明该反应己达到平衡状态的是____。
A.气体颜色不再变化
B.气体密度不再变化
C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向该容器中加入l.0mol NO2和l.0molCO,在t1时反应再次达到平衡,则N02的转化率比原平衡____(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= _____(保留两位有效数字)。
(____) N2O4与NO2之间存在反应N2O4(g) ![]() 2NO2(g )。将一定量的N2O4放入恒容密闭容器中,在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系:v(N2O4)=klp(N2O4),v(NO2)=k2P2(NO2),其中k1、k2是与反应温度有关的常数。则一定温度下,k1、k2与平衡常数Kp的关系是k1=_____。(Kp为平衡分压代替平衡浓度计算所得的平衡常数,分压=总压×物质的量分数)
2NO2(g )。将一定量的N2O4放入恒容密闭容器中,在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系:v(N2O4)=klp(N2O4),v(NO2)=k2P2(NO2),其中k1、k2是与反应温度有关的常数。则一定温度下,k1、k2与平衡常数Kp的关系是k1=_____。(Kp为平衡分压代替平衡浓度计算所得的平衡常数,分压=总压×物质的量分数)
(4)电解法处理氮氧化合物是目前大气污染治理的一个新思路,原理是将NOx在电解池中分解成无污染的N2除去,如图示,两电极间是固体氧化物电解质,在一定条件下可自由传导 O2-,如果NOx为NO,则电解池阴极电极反应式为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是.( )

A. 若直流电源 a 为负极,b 为正极,关闭 K2 ,打开 K1,一段时间后,再关闭K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒
B. 关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧杯,向试管内滴 入酚酞,发现左侧试管内溶液变红色,则 a 为负极,b 为正极
C. 若关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多则a为正极,b为负极
D. 若直流电源 a 为负极,b 为正极,关闭 K2,打开 K1,一段时间后,再关闭 K1,打开 K2,则左 侧石墨棒上发生的电极反应为 H2﹣2e﹣+2OH﹣═2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则

(1)电源A极是____极.
(2)2分钟后,若将乙池恢复到电解前的状态,则应加入______,加入的物质的量为______mol。
(3)丙池中发生反应的离子方程式为:________________
(4)丙装置上某极可析出固体___克,溶液的n(H+)为_____.
(5)电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为______mol/L.(不考虑溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A. H+(aq)+OH-(aq)===H2O(l) ΔH=-a kJ· mol-1,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为a kJ
B. 常温下,将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
C. 镀锌钢管破损后,负极反应式为Fe-2e-===Fe2+
D. 把碳酸氢钠溶液蒸干灼烧,最后得到的固体产物是碳酸氢钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积固定不变的密闭容器中进行反应:2X(g)+Y(g)![]() 2Z(g)+W(s),已知将2molX和1 molY充入该容器中,反应在某温度下达到平衡时,Z的物质的量为p mol。下列说法中正确的是( )
2Z(g)+W(s),已知将2molX和1 molY充入该容器中,反应在某温度下达到平衡时,Z的物质的量为p mol。下列说法中正确的是( )

A. 若把2molX和1 molY充入该容器时,处于状态Ⅰ,达到平衡时处于状态Ⅱ(如图1所示),则该反应的正反应是吸热反应
B. 若维持该题条件不变,仅从生成物开始配比,要求达到平衡时,Z的物质的量仍为 p mol,则W的起始物质的量n(W)应满足的条件是n(W)>(1-0.5p) mol
C. 反应达到平衡后,再将2molX和1 molY充入该容器中,则反应速率V与时间t关系图如图2所示
D. 若降低原平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的密度未发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯塑料在生产、生活中有广泛应用,其单体可由乙苯和二氧化碳在一定条件下反应制得,其反应原理如下:
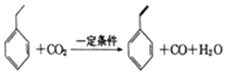
下列有关说法不正确的是
A. 苯乙烯可通过加聚反生成聚苯乙烯
B. 苯乙烯分子中所有原子可能共平面
C. 乙苯、苯乙烯均能使溴水褪色,且其褪色原理相同
D. 等质量的聚苯乙烯与苯乙烯中所含的碳原子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com