
| A、①②⑤ | B、③④⑥ |
| C、⑥⑦⑧ | D、④⑤⑧ |


科目:高中化学 来源: 题型:
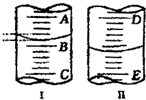 (1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是
(1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=9 |
| B、c(OH-)≈10-5mol?L-1. |
| C、pH≈7 |
| D、c(OH-)≈10-8 mol?L-1. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3kJ |
| ② | 0.8 | 2.4 | 0.4 | 放热Q kJ |
| A、容器①、②中反应达平衡时XY3的平衡浓度相同 |
| B、容器①、②中达到平衡时各物质的百分含量相同 |
| C、达平衡时,两个容器中XY3的物质的量浓度均为2 mol?L-1 |
| D、若容器①体积为0.20 L,则达平衡时放出的热量大于46.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
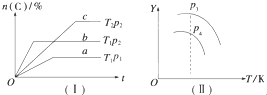 在某一容积可变的密闭容器中,可逆反应A(g)+B(g)?xC(g)△H,符合图象(Ⅰ)所示关系.由此推断,对图象(Ⅱ)的说法不正确的是( )
在某一容积可变的密闭容器中,可逆反应A(g)+B(g)?xC(g)△H,符合图象(Ⅰ)所示关系.由此推断,对图象(Ⅱ)的说法不正确的是( )| A、p3>p4,Y轴表示A的转化率 |
| B、p3>p4,Y轴表示B的质量分数 |
| C、p3>p4,Y轴表示混合气体的密度 |
| D、p3>p4,Y轴表示混合气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
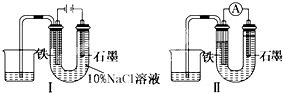 用如图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升.下列说法正确的是( )
用如图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升.下列说法正确的是( )| A、用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e-+2OH-=Fe(OH)2 |
| B、装置Ⅰ通电10分钟后铁电极周围溶液pH降低 |
| C、用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e-=H2↑ |
| D、同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将1.0molFeCl3全部制成胶体,其中氢氧化铁胶粒为NA个 |
| B、常温常压下,16 g氧气和臭氧(O3)的混合气体中含有NA 个氧原子 |
| C、12g NaHSO4在熔融时离子总数为0.3NA个 |
| D、标准状况下,11.2L氦气所含的原子数为NA个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com