
【题目】化合物Ⅳ为一种重要化工中间体,其合成方法如下: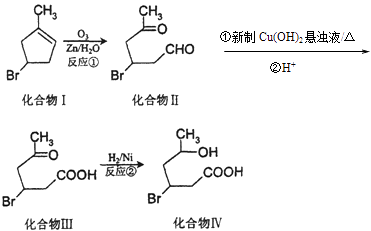
(1)化合物Ⅰ在核磁共振氢谱图吸收峰个数为;反应②的反应类型为 .
(2)化合物Ⅱ与新制Cu(OH)2悬浊液反应,写出该反应的化学方程式 .
(3)化合物I在NaOH醇溶液中加热反应得到化合物X,X的结构简式可能是 . (写出任意一种的结构简式).
(4)化合物III与足量NaOH水溶液加热反应的化学方程式为 .
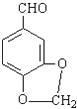
(5)异黄樟油素 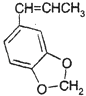 发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
(6)有关上述化合物,说法不正确的是
A.1mol化合物Ⅲ,最多可与2molH2反应
B.化合物Ⅳ在一定条件下能与HBr反应
C.化合物Ⅰ能使酸性高锰酸钾溶液褪色
D.化合物Ⅳ在一定条件下能发生缩聚反应
E.化合物Ⅱ分子式为C6H11O2Br.
【答案】
(1)5;加成反应(或还原反应)
(2)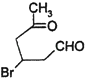 +2Cu(OH)2
+2Cu(OH)2![]()
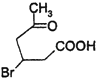 +Cu2O↓+2H2O
+Cu2O↓+2H2O
(3)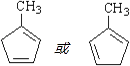
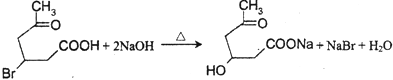
(4)
(5)
(6)AE
【解析】解:(1)根据化合物Ⅰ的结构简式可知,其分子中含有5种等效H,则核磁共振氢谱图吸收峰个数为5;反应②中C=O变成C﹣O键,该反应属于加成反应,也属于还原反应,所以答案是:5;加成反应(或还原反应);(2)化合物Ⅱ为 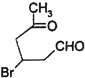 ,其分子中含有醛基,能够与新制氢氧化铜浊液发生反应生成
,其分子中含有醛基,能够与新制氢氧化铜浊液发生反应生成 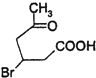 ,反应的化学方程式为:
,反应的化学方程式为:  +2Cu(OH)2
+2Cu(OH)2![]()
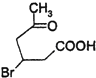 +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
所以答案是: 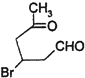 +2Cu(OH)2
+2Cu(OH)2![]()
 +Cu2O↓+2H2O;(3)化合物I在NaOH的醇溶液中反应发生消去反应,可得到两种有机物,结构简式分别为:
+Cu2O↓+2H2O;(3)化合物I在NaOH的醇溶液中反应发生消去反应,可得到两种有机物,结构简式分别为: 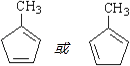 ,
,
所以答案是: 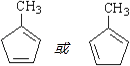 ;(4)化合物III中含有﹣COOH和﹣Br,在碱性条件下反应生成﹣COONa和﹣OH,则反应的方程式为:
;(4)化合物III中含有﹣COOH和﹣Br,在碱性条件下反应生成﹣COONa和﹣OH,则反应的方程式为: 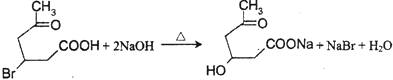 ,
,
所以答案是: 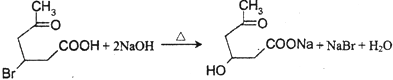 ;(5)异黄樟油素(
;(5)异黄樟油素( 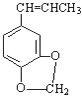 )发生类似反应①的反应,应为C=C被氧化分别生成醛或酮,则生成的化合物Ⅵ的结构简式为:
)发生类似反应①的反应,应为C=C被氧化分别生成醛或酮,则生成的化合物Ⅵ的结构简式为: 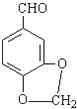 ,
,
所以答案是:  ;(6)A.1mol化合物Ⅲ(
;(6)A.1mol化合物Ⅲ( 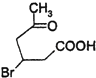 )中含有1mol碳碳双键,最多可与1molH2反应,故A错误;
)中含有1mol碳碳双键,最多可与1molH2反应,故A错误;
B.化合物Ⅳ中含有羟基,在一定条件下能与HBr发生取代反应,故B正确;
C.化合物Ⅰ中含有碳碳双键,能被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,故C正确;
D.化合物Ⅳ中含有羟基和羧基,在一定条件下能发生缩聚反应生成高分子化合物,故D正确;
E.根据化合物Ⅱ的结构简式可知,其分子式为C6H9O2Br,故E错误;
所以答案是:AE.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下: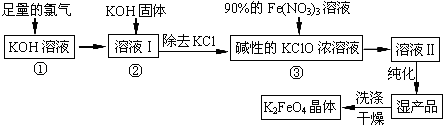
(1)反应①应在温度较低的情况下进行.因在温度较高时KOH 与Cl2 反应生成的是KClO3 . 写出在温度较高时KOH 与Cl2反应的化学方程式 , 该反应的氧化产物是 .
(2)在溶液Ⅰ中加入KOH固体的目的是(填编号).
A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 .
(4)如何判断K2FeO4晶体已经洗涤干净 .
(5)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.FeO42﹣在水溶液中的存在形态如图Ⅱ所示.下列说法正确的是(填字母). 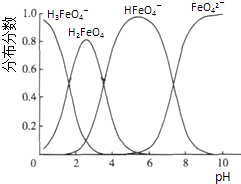
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4﹣的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH﹣═HFeO4﹣+H2O.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,M、N 两种气体的物质的量随时间变化的曲线如图所示:

(1)反应的化学方程式为_______________。
(2)反应达到最大限度的时间是______min,该时间内的平均反应速率v(N)=______。
(3)反应达到平衡状态时,放中6QkJ的热量,当容器中充入lmolN,反应放出的热量为_____。
①等于QkJ ②小于QkJ ③大于QkJ ④等于2QkJ
(4)判断该反应达到平衡状态的依据是__________。
①该条件下,正逆反应速率都为零
②该条件下,混合气体的密度不再发生变化
③该条件下,混合气体的压强不再发生变化
④该条件下,单位时间内消耗2molN的同时,生成1molM
(5)能能加快反应速率的措施是_________。
①升高温度 ②容器体积不变,充入隋性气体Ar
③容器压強不变,充入惰性气体Ar ④使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2 ![]() 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( ) ①单位时间内生成n mol O2的同时生成2n mol NO2
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( ) ①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态.
A.①④⑥⑦
B.②③⑤⑦
C.①③④⑤
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( ) 
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.非金属性:X<Z
D.M元素最高价氧化物对应水化物具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D都是中学化学中常见的有机化合物,它们在一定的条件下有如下转化关系(部分物质和条件被略去).其中,A是最简单的烯烃,分子式为C2H4 , 其产量可用来衡量一个国家石油化工发展的水平.C是生活中常用的一种具有酸味的调味品的成分;通常状况下,D是具有浓郁香味的油状液体. 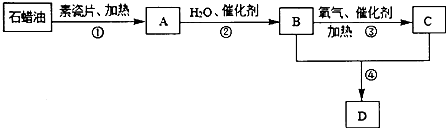
(1)在有机化合物A,B,C,D中,属于烃类的是(填结构简式);反应④的反应类型是 .
(2)在A,B,C,D中,密度比水小且难溶于水的液体是(填物质名称).A在一定条件下可以发生加聚反应生成一种塑料,该塑料的结构简式为 .
(3)反应①中,素瓷片的主要作用是 . 一定条件下, B,C,D三种物质中不能和NaOH溶液反应发生反应的是(填物质名称).
(4)植物秸秆在一定条件下能水解成葡萄糖,葡萄糖在酒化酶的作用下能转化为B,B在某种微生物存在下发生氧化反应得到C.写出葡萄糖转化为B的化学方程式: .
(5)在实验室获得的D中往往含有少量的B,C;为提纯D,可以先将此不纯的D和一充分混合,然后再静置、(填操作名称)即可.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知β锂辉矿(主要成分为LiAlSi2O6 , 还含有FeO、MgO、CaO等杂质),下面是以锂辉矿为原料来制取金属锂的一种工艺流程.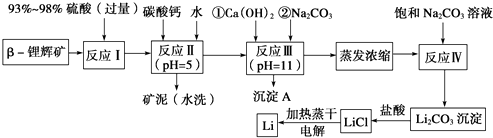
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)为了提高β锂辉矿浸出率可采取措施有 .
(2)反应Ⅰ发生主反应:LiAlSi2O6+H2SO4(浓Li2SO4+++H2O,根据题意配平上述方程式.
(3)反应Ⅱ加入碳酸钙的作用是 .
(4)反应Ⅲ中生成沉淀A成分: . (填化学式)
(5)蒸发浓缩过程中主要发生离子反应方程式: .
(6)洗涤所得Li2CO3沉淀要使用(选填“热水”或“冷水”),你选择的理由是 .
(7)电解熔融氯化锂生产锂时,阳极产生的Cl2中会混有少量O2 , 用电极反应式说明原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的锌与100mL 18.5mol/L H2SO4充分反应后,锌完全溶解,同时生成气体A 22.4L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
A.气体A为SO2和H2的混合物
B.反应中共消耗Zn 65g
C.气体A中SO2和H2的体积比为1:4
D.反应中共转移电子2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的离子方程式
(1)碳酸钙与稀盐酸混合 ______________________________。
(2)铝与氢氧化钠溶液反应 ______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com