
【题目】羟胺的电离方程式为:NH2OH+H2O![]() NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
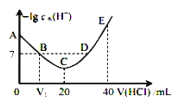
A.图中V1<10
B.A点对应溶液的pH=9.5
C.A、B、C、D四点中酸性最强的点为C点
D.E点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+2c(NH2OH)
【答案】C
【解析】
A.羟胺是一元弱碱,若V1=10,则反应恰好起始时产生等量的NH2OH和NH3OH+,由Kb=9.0×10-9得到![]() 即NH3OH+的水解比NH2OH电离程度大,溶液呈酸性,而A点时水的电离达到107 molL1,说明NH3OH+的水解程度和NH2OH抑制水的程度相当,因此NH3OH+物质的量浓度要小于NH2OH物质的量浓度,故滴加的HCl小于10mL,所以V1应<10,故A正确;
即NH3OH+的水解比NH2OH电离程度大,溶液呈酸性,而A点时水的电离达到107 molL1,说明NH3OH+的水解程度和NH2OH抑制水的程度相当,因此NH3OH+物质的量浓度要小于NH2OH物质的量浓度,故滴加的HCl小于10mL,所以V1应<10,故A正确;
B.羟胺的电离方程式为:NH2OH+H2O![]() NH3OH++OH,已知25℃时,其电离平衡常数为Kb=9.0×109,
NH3OH++OH,已知25℃时,其电离平衡常数为Kb=9.0×109,![]() ,
,![]() ,pOH = 4.5,pH = 144.5 =9.5,故B正确;
,pOH = 4.5,pH = 144.5 =9.5,故B正确;
C.A点是NH2OH ,溶液显碱性,B点溶液产生NH3OH+水解,水解程度等于NH2OH的电离程度,溶液呈中性,C点只有一种溶质,NH3OH+水解显酸性,D点溶液HCl过量,溶液呈酸性,因此酸性最强的是D电,故C错误;
D.E点时加入HCl的体积为40mL,根据电荷守恒:c(H+)+c(NH3OH+)=c(OH)+c(Cl),根据物料守恒:2c(NH3OH+)+2c(NH2OH)=c(Cl),则有c(H+)=c(OH)+c(NH3OH+)+2c(NH2OH),故D正确。
综上所述,答案为C。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,1LC2H5OH完全燃烧后生成的CO2分子个数约为![]()
B.20gD2O与20gH218O含有的中子数均为10NA
C.1mol·L-1Al(NO3)3溶液中含有3NA个NO3-
D.50mL12mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
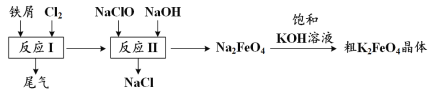
下列叙述不正确的是
A.用K2FeO4对饮用水杀菌消毒的同时,还产生Fe(OH)3胶体吸附杂质净化水
B.用FeCl2溶液吸收反应I中尾气后可再利用
C.反应II中氧化剂与还原剂的物质的量之比为3∶2
D.该生产条件下,物质的溶解性:Na2FeO4< K2FeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)26H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
(资料1)
沉淀 | Fe(OH)2 | Fe(OH)3 |
开始沉淀 pH | 7.6 | 2.7 |
完全沉淀 pH | 9.6 | 3.7 |
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________。
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
实验1 | pH=1 | pH=5 | 8.4 |
实验2 | pH=1 | pH=1 | 6.5 |
实验3 | pH=6 | pH=5 | 7.8 |
实验4 | pH=6 | pH=1 | 5.5 |
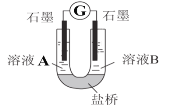
(资料2)原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
(资料3)常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对(资料3)实验事实的解释为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某化工厂以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分Na2Cr2O7·2H2O),工艺流程如图:
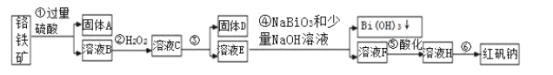
i.常温,NaBiO3不溶于水,有强氧化性,碱性条件下,能将Cr3+转化为CrO42-。
ii.常温时,部分金属离子开始沉淀和完全沉淀时的pH值
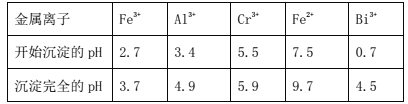
(1)步骤①提高酸溶速率的措施__(任填一条即可)。固体A的成分是___。
(2)步骤③需加氢氧化钠溶液调节pH,调节pH范围为__,目的是__。
(3)写出④反应的离子方程式__。
(4)将溶液H经过__即得红矾钠粗晶体。
Ⅱ.经该工厂的工业废水中含1.00×10-3mol·L-1的Cr2O72-,其毒性较大。该化工厂的科研人员为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价依次为+3、+2),又设计了如下工艺流程:
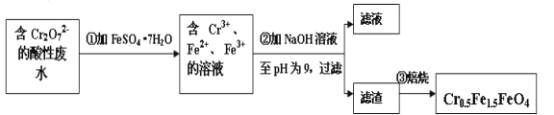
(5)第①步反应的离子方程式是__。
(6)常温时,如忽略步骤①所加FeSO4·7H2O所引起的溶液体积变化,依据上表数据,则步骤②加入NaOH溶液调节溶液的pH至9时,溶液中Cr3+的浓度为___mol/L(101/2≈3.2)。
(7)欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4。理论上需要加入FeSO4·7H2O的质量为__g(已知FeSO4·7H2O的摩尔质量为278g/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、铁、铝是应用最广泛的三种金属。
(1)它们在人类的金属使用历史中,由早到晚的顺序为__________________________。
(2)日常常用“铝壶”烧开水,是因为铝有良好的导热性、__________________________。
(3)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式________________________________________________,该反应是_______ (填:吸或放)热反应,其中铝发生________(填:氧化或还原)反应。
(4)表面破损的铝制品,放久了破损处会有一层“白毛”产生,“白毛”既能溶于酸又能溶于碱溶液,写出形成“白毛”的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属有机多孔材料FJI-H14在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法不正确的是( )
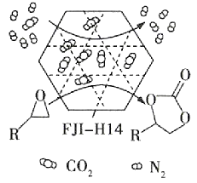
A.该材料的吸附作用具有选择性
B.该方法的广泛使用有助于减少CO2排放
C.在生成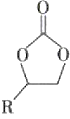 的过程中,有极性共价键形成
的过程中,有极性共价键形成
D.其工作原理只涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I是一种医药合成中间体,实验室以芳香烃A为原料制备I的路线如图(部分反应条件已省略):

已知:RCH=CH2+HBr![]() RCH2CH2Br。
RCH2CH2Br。
回答下列问题:
(1)X的分子式为C8H8,且X与A互为同系物,则X的化学名称是___。
(2)B生成C的反应类型是___,B、C含有的相同的官能团名称是___。
(3)碳原子上连有4个不同原子或基团时,该碳原子为手性碳原子。写出D的结构简式,并用星号(*)标出其中的手性碳原子___。
(4)设计实验检验有机物E中的含氧官能团:___。
(5)G的结构简式是___。
(6)Y与C是同分异构体,Y中含苯环,且苯环上有2个取代基,Y能发生银镜反应,其核磁共振氢谱中有5组峰,且峰面积之比为6:2:2:1:1,则Y的结构简式为___。
(7)丙二酸(HOOCO2COOH)主要用作医药合成中间体、电镀抛光剂等。设计以丙烯(CH3CH=CH2)和 为原料制备丙二酸的合成路线:___(无机试剂任选)。
为原料制备丙二酸的合成路线:___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物具有抗癌抑菌活性,其结构如图所示,下列关于该有机物说法正确的是( )

A.该有机物可以使溴水、酸性高锰酸钾溶液褪色,遇FeCl3溶液会显紫色
B.该有机物结构中含5个手性碳原子
C.1mol该有机物最多和4molH2反应
D.1mol该有机物最多消耗1molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com