

 ;G的结构简式HCOOCH3;
;G的结构简式HCOOCH3; .写出D与C反应生成A的化学方程式CH3OH+
.写出D与C反应生成A的化学方程式CH3OH+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 分析 A在氢氧化钠水溶液、加热水解生成B与C,A中含有酯基,C氧化生成E,E氧化生成F,则C为醇、E为醛、F为羧酸,E常温下为气体,则E为HCHO,故C为CH3OH、F为HCOOH.C与F在浓硫酸作用下发生酯化反应生成G,则G为HCOOCH3.
B酸化得到D,D与碳酸氢钠反应生成H,H为气体,则H为CO2,D中含有羧基,化合物D能使FeCl3溶液显紫色,则D还含有酚羟基,化合物A苯环上取代时可生成两种一取代物,苯环上含有2种H原子,结合A的分子式C8H8O3中C原子数目可知,A含有2个取代基为-OH、-COOCH3且处于对位,故A为 、B为
、B为 、D为
、D为 ,据此分析解答.
,据此分析解答.
解答 解:A在氢氧化钠水溶液、加热水解生成B与C,A中含有酯基,C氧化生成E,E氧化生成F,则C为醇、E为醛、F为羧酸,E常温下为气体,则E为HCHO,故C为CH3OH、F为HCOOH.C与F在浓硫酸作用下发生酯化反应生成G,则G为HCOOCH3.
B酸化得到D,D与碳酸氢钠反应生成H,H为气体,则H为CO2,D中含有羧基,化合物D能使FeCl3溶液显紫色,则D还含有酚羟基,化合物A苯环上取代时可生成两种一取代物,苯环上含有2种H原子,结合A的分子式C8H8O3中C原子数目可知,A含有2个取代基为-OH、-COOCH3且处于对位,故A为 、B为
、B为 、D为
、D为 ,
,
(1)由上述分析可知,A为 ,其官能团名称是酯基和酚羟基,F为HCOOH,官能团名称是羧基;D为
,其官能团名称是酯基和酚羟基,F为HCOOH,官能团名称是羧基;D为 ,G为HCOOCH3,
,G为HCOOCH3,
故答案为:酯基和酚羟基;羧基; ;HCOOCH3;
;HCOOCH3;
(2)反应(I)属于水解反应;反应(Ⅱ)属于酯化反应,故答案为:水解反应;酯化反应;
(3)C→E的化学方程式为:2CH3OH+O2$→_{△}^{催化剂}$2HCHO+2H2O;
D→H的化学方程式为: ,
,
D+C→A的方程式,CH3OH+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:2CH3OH+O2$→_{△}^{催化剂}$2HCHO+2H2O; ;CH3OH+
;CH3OH+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O.
点评 本题考查有机物推断,为高频考点,以分子式、反应条件及题给信息进行推断,侧重考查学生分析推断能力,正确判断A的结构是解本题关键,注意只有羧基能和碳酸氢钠反应,题目难度中等.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
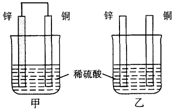
| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中硫酸溶液的浓度均下降 | D. | 产生气泡的速度甲比乙慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②⑤⑥ | C. | ② | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
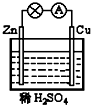
| A. | 正极反应为 Cu-2e-Cu2+ | B. | 溶液中H+向锌片移动 | ||
| C. | 电子由锌片通过导线流向铜 | D. | 该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com