
【题目】通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,负极反应的物质为 ,正极反应的物质为 ,酸式电池的电极反应:
负极: ,正极: 。
电解质溶液pH的变化 (填“变大”,“变小”,“不变”)。
(2)在碱式介质中,碱式电池的电极反应:
负极: ,正极: 。
电解质溶液pH的变化 (填“变大”,“变小”,“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是________。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式相同
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
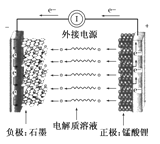
①该电池放电时负极反应式为_________________。
②放电时每转移3 mol电子,正极有________ mol K2FeO4被还原。
锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。
电池反应式为:Li1-xMnO4+Lix ![]() LiMnO4,下列有关说法不正确的是________。
LiMnO4,下列有关说法不正确的是________。
A.放电时电池的正极反应式为:Li1-xMnO4+xLi++xe-===LiMnO4
B.放电过程中,石墨没有得失电子
C.该电池也能在KOH溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
【答案】(1)H2;O2;2H2-4e-=4H+;O2+4e-+4H+=2H2O;变大
(2)2H2-4e-+4OH-=2H2O;O2+4e-+2H2O=4OH-;变小
(3)C
(4)Zn-2e-+2OH-═Zn(OH)2;1
(5)C
【解析】
试题分析:(1)在酸性氢氧燃料电池中,石墨作电极,负极是氢气失电子生成氢离子,电极反应为2H2-4e-=4H+;正极是氧气得电子生成氢氧根离子,生成的氢氧根离子结合氢离子生成水,电极反应为O2+4e-+4H+=2H2O,由于正负极消耗与生成的氢离子等量,所以氢离子的总量不变,而总电极反应式为2H2+O2=2H2O,水的总量增加,氢离子浓度减小,pH变大;
(2)在碱式介质中,氢气在负极失去电子生成氢离子,氢离子结合氢氧根离子生成水,电极反应式为2H2-4e-+4OH-=2H2O;氧气在正极得电子生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,由于正负极消耗与生成的氢氧根离子等量,所以氢氧根离子的总量不变,而总电极反应式为2H2+O2=2H2O,水的总量增加,氢氧根浓度减小,pH变小;
(3)A、电解获得H2消耗较多的能量,而在催化剂作用下利用太阳能来分解H2O获得H2更为科学,A正确;B、氢氧燃料电池产物H2O无污染,能有效保护环境,B正确;C、以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式分别为:H2-2e-=2H+,H2-2e-+2OH-=H2O,不相同,C错误;D、以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式均为2H2+O2=2H2O,D正确,答案选C。
(4)①放电时,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-+2OH-═Zn(OH)2;
②放电时,正极上1molK2FeO4得3mol电子发生还原反应生成1molFe(OH)3,所以每转移3 mol电子,正极有1molK2FeO4被还原;
(5)A、根据总反应式可知Li失去电子,电池负极反应式为:xLi-xe-═xLi+,由总反应式减去负极反应式可得放电时的正极反应式为Li1-xMnO4+xLi++xe-===LiMnO4,A正确;B、放电过程中,根据总反应式Li1-xMnO4+Lix ![]() LiMnO4可判断石墨没有电子得失,B正确;C、Li能与KOH溶液中的H2O反应,导致电池无法正常工作,C错误;D、充电过程是放电的逆向过程,外界电源的负极提供的电子使原电池负极获得电子发生还原反应,所以标有“-”的电极应与外接电源的负极相连,D正确,答案选C。.
LiMnO4可判断石墨没有电子得失,B正确;C、Li能与KOH溶液中的H2O反应,导致电池无法正常工作,C错误;D、充电过程是放电的逆向过程,外界电源的负极提供的电子使原电池负极获得电子发生还原反应,所以标有“-”的电极应与外接电源的负极相连,D正确,答案选C。.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】现有前四周期原子序数依次递增的五种元素A、B、C、D、E。 A、D元素基态原子中成对电子数是未成对电子数的3倍,且D元素基态原子中有6个未成对电子;B的基态原子核外只有7个原子轨道填充了电子,B、C元素基态原子的3p能级上均有1个未成对电子;E元素排在周期表的15列。
(1)B元素基态原子核外电子有_______种运动状态,电子占据的最高能层符号为_______,该能层具有的原子轨道数为_______、电子数为_____。
(2)C、E两元素可以形成化合物EC3,此化合物的VSEPR模型为_______,是_______分子(填“极性”、“非极性”)。
(3)写出D基态原子的外围电子排布图____________。
(4)B、C两元素也可以形成共价化合物BC3,但BC3经常以二聚(B2C6)的形式存在,二聚分子具有配位键,分子中原子间成键的关系如下图所示.请将图中,你认为是配位键的斜线上加上箭头。
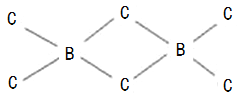
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 Ⅰ.按己知的原子结构规律,82号元素X应是第_________周期_________族元素,它的最高正价氧化物的化学式为_________。
Ⅱ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解。用序号填空:
(1)未破坏化学键的是_____________。
(2)仅离子键被破坏的是_____________。
(3)仅共价键被破坏的是_____________。
Ⅲ.有下列各组物质:①石墨和足球烯C60;②126C和136C;③CH3—CH2—CH2—CH3和CH3—CH(CH3)CH3;④漂白粉和漂白液主要成分;⑤正丁烷和异庚烷;⑥乙烯和聚乙烯;⑦![]() 和
和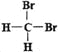 ;⑧丙烷和环丙烷。用序号填空:
;⑧丙烷和环丙烷。用序号填空:
(1)__________组两者互为同位素。(2)__________组两者互为同素异形体。
(3)__________组两者属于同系物。(4)__________组两者互为同分异构体。
(5)__________组两者是同一物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是 。
② 氨催化氧化生成一氧化氮反应的化学方程式是 。
(2)氨的定量检测。
水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:
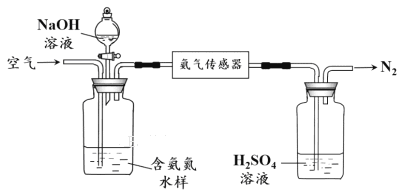
① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用: 。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol ,则水样中氨氮(以氨气计)含量为 mg·L-1。
(3)氨的转化与去除。
微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
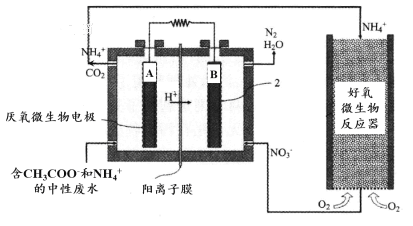
① 已知A、B两极生成CO2和N2,写出A极的电极反应式: 。
② 用化学用语简述NH4+去除的原理: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D原子序数之和是C的原子序数的1.5倍。
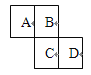
(1)写出A、B、C、D的元素符号:A 、B 、
C 、D 。
(2)A、B、C、D的气态氢化物最不稳定的是(写化学式) 。
(3)A、D两元素的气态氢化物相互反应的化学方程式为 ,现象为 ,产物为 化合物(填“离子”或“共价”)。该化合物中存在的化学键有 (填“离子键”或“共价键”)。
(4)写出下列电子式:
D的气态氢化物 ,A单质 。B的气态氢化物的形成过程用电子式表示: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态钛原子的价电子排布图为
(2)已知TiCl4在通常情况下是无色液体,熔点为﹣37℃ ,沸点为136℃ ,可知TiCl4为 晶体.
(3)硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示。该阳离子Ti与O的原子数之比为 。
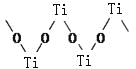
(4)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的钴原子有 个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成是 。


(5)由C、Mg、Ni三种元素组成的一种简单立方结构的化合物具有超导性,其晶胞中C位于体心位置,Mg位于顶角,Ni占据面心位置,该化合物的化学式为 ,晶体中Mg原子周围距离最近的Ni原子有 个,该新型超导材料晶胞参数a=0.38nm,计算该晶体的密度 (gcm﹣3)(保留三位有效数字)
(6)金属钛晶胞结构如图所示,设钛原子的半径为r,则该晶胞体积的表达式为

查看答案和解析>>
科目:高中化学 来源: 题型:
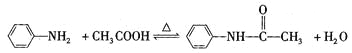
【题目】乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂和防腐剂、乙酰苯胺的制备原理为
实验参数
名称 | 相对分 | 性状 | 密度(g/mL) | 沸点( | 溶解性 | |
苯胺 | 93 | 无色油状液体 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,可溶于热水 | 易溶于乙醇、乙醚 |
实验装置如图所示(部分仪器及夹持装置已略去)。
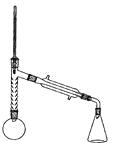
注:①刺型分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。②苯胺易被氧化。
实验步骤:
步骤1:在100mL圆底烧瓶中加入无水苯胺9.3mL、冰醋酸18.4mL、锌粉0.1g和少量沸石,安装好仪器后,对圆底烧瓶均匀加热,使反应液在微沸状态下回流,调节加热温度,使温度计温度控制在105![]() 左右;反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
左右;反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步骤2:在搅拌下,趁热将蒸馏烧瓶中的液体以细流状倒入盛有冰水的100mL烧杯中,快速搅拌,乙酰苯胺结晶析出,烧杯内试剂冷却至室温后,进行抽滤、洗涤、干燥,可得到乙酰苯胺粗品。
步骤3:将乙酰苯胺粗品进行重结晶,待结晶完全后抽滤,尽量压甘干滤饼。将产品置于干净的表面皿中晾干,称重,计算产率、
请回答下列问题:
(1)实验中加入锌粉的目的是_____________________。
(2)从化学平衡的角度分析,控制温度计的温度在105![]() 左右的原因是______________。
左右的原因是______________。
(3)通过_____________可判断反应基本完成、
(4)步骤1加热可用_____________(填“水浴”或“油浴”)。
(5)洗涤乙酰苯胺粗品最合适的方法是__________________(填字母)。
A.用少量冷水洗
B.用少量热水洗
C.先用冷水洗,再用热水洗
D.用酒精洗
(6)步骤2得到的粗品中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗品用热水溶解,加入活性炭0.1g,煮沸进行脱色,______________,再将滤液冷却结晶。
(7)该实验最终得到产品9.1g,则乙酰苯胺的产率是____________(小数点后保留两位数字。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势,如图所示:
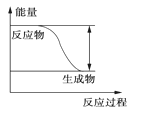
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_____(填字母)。
A.改铁片为铁粉 B.增大压强
C.升高温度 D.改稀硫酸为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”)。铜片上产生的现象为________________;该极上发生的电极反应为______________;外电路中电子由 _______极向_______极移动。(填“正”或“负”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题:
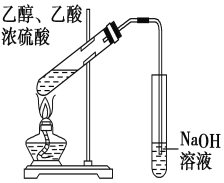
(1)写出制取乙酸乙酯的化学反应方程式 。
(2)浓硫酸的作用是: 。
(3)实验装置图有明显错误,请指出错误是 。
(4)实验中可以观察到的现象是________________________ _____________ 。
(5) 写出把制得的乙酸乙酯分离出来所需的试剂和方法 。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
②单位时间里,生成1mol乙酸乙酯,同时生成1mol水
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④混合物中各物质的浓度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com