


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
| A、晶体中有阳离子就一定存在阴离子 |
| B、原子晶体中,一定只存在共价键 |
| C、金属晶体的熔点一定比分子晶体高 |
| D、分子晶体中一定存在共价键和分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| A、NH3分子中N原子采用sp2杂化 |
| B、相同压强时,NH3沸点比PH3高 |
| C、[Cu(NH3)4]2+离子中,N原子是配位原子 |
D、CN-的电子式为: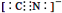 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com