
| A. | 将苯与浓硝酸、浓硫酸的混合物在60℃水浴加热条件下反应可生成硝基苯 | |
| B. | 用酸性高锰酸钾可以检验CH2=CH-CHO中碳碳双键 | |
| C. | 将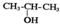 与NaOH的醇溶液共热制备CH3-CH=CH2 与NaOH的醇溶液共热制备CH3-CH=CH2 | |
| D. | 向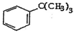 中通入足量的酸性高锰酸钾溶液可以得到 中通入足量的酸性高锰酸钾溶液可以得到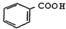 |
分析 A.在60℃水浴加热、浓硫酸作催化剂条件下,苯和浓硝酸发生取代反应;
B.醛基和碳碳双键都能被酸性高锰酸钾溶液氧化;
C.醇在浓硫酸作催化剂加热条件下发生消去反应生成烯烃;
D.连接苯环的碳原子上含有H原子的苯的同系物能被酸性高锰酸钾溶液氧化生成苯甲酸.
解答 解:A.在60℃水浴加热、浓硫酸作催化剂条件下,苯和浓硝酸发生取代反应生成硝基苯,该反应也是硝化反应,故A正确;
B.醛基和碳碳双键都能被酸性高锰酸钾溶液氧化,所以不能用酸性高锰酸钾溶液检验碳碳双键,应该先将醛基转化为羧基,然后再检验碳碳双键,故B错误;
C.醇在浓硫酸作催化剂加热条件下发生消去反应生成烯烃,卤代烃和氢氧化钠醇溶液共热发生消去反应生成烯烃,故C错误;
D.连接苯环的碳原子上含有H原子的苯的同系物能被酸性高锰酸钾溶液氧化生成苯甲酸, 中连接苯环的碳原子上不含氢原子,则不能被酸性高锰酸钾溶液氧化生成苯甲酸,故D错误;
中连接苯环的碳原子上不含氢原子,则不能被酸性高锰酸钾溶液氧化生成苯甲酸,故D错误;
故选A.
点评 本题考查实验方案评价,为高频考点,明确物质结构和性质关系是解本题关键,涉及官能团检验、物质性质,注意B中醛基也能被酸性高锰酸钾、溴氧化,注意苯的同系物被酸性高锰酸钾溶液氧化的结构特点,易错选项是D.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:
黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 “即食即热型快餐”适合外出旅行时使用.其内层是用铝箔包裹的并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
“即食即热型快餐”适合外出旅行时使用.其内层是用铝箔包裹的并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )| A. | 氢氧化钡晶体和氯化铵晶体 | B. | 生石灰与水 | ||
| C. | 金属钠与水 | D. | 氯化钠与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其它物质 |
| Ⅰ | 2mL | 20 | / |
| Ⅱ | 2mL | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2mL | 30 | / |
| Ⅳ | 1mL | 20 | 1mL蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲正确 | B. | 乙正确 | C. | 甲、乙均正确 | D. | 甲、乙均不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、H2S、PH3的稳定性依次增强 | |||||||||||||||
| B. | 按Mg、Si、N、F的顺序,原子半径由小变大 | |||||||||||||||
| C. | 某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第ⅤA族
| |||||||||||||||
| D. | 在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
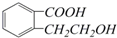 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质: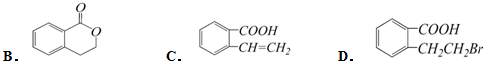
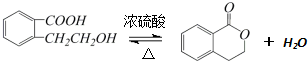 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com