
【题目】氯气是一种有毒的气体,工业上常用浓氨水挥发出来的氨气检验氯气管道是否漏气,某学生为探究此反应原理,设计如下实验,请回答下列问题:

(1)选择上图装置,填写接口顺序_________

(2)装置D中发生反应的离子化学方程式为___________;
(3)装置E、F的作用分别是_________;__________。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物为单质。写出反应的化学方程式:________;此时F中发生的离子方程式为___________。
(5)氯气程式与与氨气在水溶液中可以反应生成氯胺(NH2Cl),氯胺是一种长效缓释的杀菌消毒剂,写出氯胺与水反应的化学反应方程:___________。
【答案】 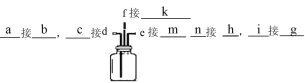 MnO2+4H++2Cl-
MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O E装置的作用是除去氯气中的杂质气体HCl F装置吸收多余的尾气 8NH3+3Cl2=6NH4Cl+N2 Cl2+HSO3-+H2O=2Cl-+3H++SO42- NH2Cl+H2O=NH3+HClO(生成NH4ClO也得分)
Mn2++Cl2↑+2H2O E装置的作用是除去氯气中的杂质气体HCl F装置吸收多余的尾气 8NH3+3Cl2=6NH4Cl+N2 Cl2+HSO3-+H2O=2Cl-+3H++SO42- NH2Cl+H2O=NH3+HClO(生成NH4ClO也得分)
【解析】(1)实验室制取NH3可选择A装置利用NH4Cl和Ca(OH)2混合加热获得,再通过碱石灰干燥;氯气可选择D装置利用浓盐酸和二氧化锰混合加热获得,并借助饱和食盐水除去挥发出的HCl,利用浓硫酸干燥氯气,在C中将氯气和氨气混合,并利用亚硫酸氢钠溶液吸收多余的氯气或氨气,防止污染空气,根据气体的流向,装置连接方法为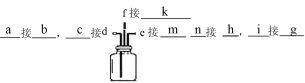 ;
;
(2)装置D中制取氯气发生反应的离子化学方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)装置E中饱和食盐水是吸收挥发出的氯气,F中亚硫酸氢钠溶液吸收多余的氯气或氨气,防止污染空气;
(4)NH3遇Cl2出现浓厚的白烟并在容器内壁凝结,说明产物为NH4Cl,同时得到的单质为N2,发生反应的化学方程式为8NH3+3Cl2=6NH4Cl+N2;因氯气有强氧化性,NaHSO3有还原性,则F中亚硫酸氢钠溶液吸收多余的氯气发生的离子方程式为Cl2+HSO3-+H2O=2Cl-+3H++SO42-;
(5)氯胺(NH2Cl)是一种长效缓释的杀菌消毒剂,是因为氯胺溶于水水解生成HClO的缘故,氯胺与水反应的化学反应方程为NH2Cl+H2O=NH3+HClO。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是
A. 用湿润的pH试纸测稀碱液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 含有相同氧原子数的SO2和CO的质量之比为7:8
B. 等物质的量浓度的盐酸与醋酸中的c(H+)相等
C. 等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等
D. 等温等压下,SO2气体与CO2气体的密度之比等于11:16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.原电池是把电能转变为化学能的装置
B.原电池中电子流出的一极是负极,发生氧化反应
C.原电池的两极发生的反应均为氧化还原反应
D.形成原电池后,原电池中的阳离子向负极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是( )
A. 苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B. 苯乙烯在合适条件下催化加氢可生成乙基环己烷
C. 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是
酸性氧化物 | 一元酸 | 强电解质 | 分散系 | |
A | Mn2O7 | 丙酸 | 三氧化二铝 | 黄河水 |
B | NO2 | 高氯酸 | 盐酸 | 有色玻璃 |
C | SiO2 | 石炭酸 | 氢氧化铝 | 云、雾 |
D | SO2 | 硝酸 | 溴化氢 | 冰水混合物 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是( )
A. Na+、K+、SO42-、HCO3-B. Cu2+、K+、SO42-、NO3-
C. Na+、K+、Cl-、NO3-D. Ca2+、K+、CO32-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com