
 B(g)+D(g)在密闭容器中分别在下列四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B(g)+D(g)在密闭容器中分别在下列四种不同的条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:| 实验序号 时间 | 0 | 2 | 3 | 4 |
| 800 | ℃ | 800 | ℃ | |
| 1 | 1.0 | c2 | c3 | 1.0 |
| 10 | 0.80 | 0.60 | 0.92 | 0.20 |
| 20 | 0.67 | 0.50 | 0.75 | 0.20 |
| 30 | 0.57 | 0.50 | 0.63 | 0.20 |
| 40 | 0.50 | 0.50 | 0.60 | 0.20 |
| 50 | 0.50 | 0.50 | 0.60 | 0.20 |
| 60 | 0.50 | 0.50 | 0.60 | 0.20 |
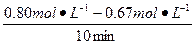 ="0.013" mol·L-1·min-1
="0.013" mol·L-1·min-1

科目:高中化学 来源:不详 题型:单选题


| A.a是反应物 |
| B.正反应是一个体积扩大的反应 |
| C.若升高温度,a的转化率增大 |
| D.若增大压强,a的转化率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法正确的是( )
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法正确的是( )| A.(m+n)必定小于p | B.(m+n)必定大于p |
| C.m必定小于p | D.m必定大于p |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3C(g)+D(s)(正反应为放热反应),图2-28中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
3C(g)+D(s)(正反应为放热反应),图2-28中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )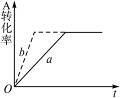
| A.增大A的浓度 | B.扩大容器的容积 |
| C.加入催化剂 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
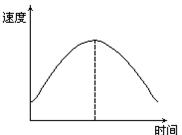
| A.①④ |
| B.③④ |
| C.①②③ |
| D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
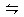 N2+3H2,并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中NH3的转化率为P%,则乙容器中NH3的转化率为( )
N2+3H2,并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中NH3的转化率为P%,则乙容器中NH3的转化率为( )| A.=P% | B.<P% | C.>P% | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 试管 | 温度 | 过氧化氢浓度 | 催化剂 |
| A | 室温(25℃) | 12% | 有 |
| B | 水浴加热(50℃) | 4% | 无 |
| C | 水浴加热( 50℃) | 12% | 有 |
| D | 室温(25℃) | 4% | 无 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验序号 | 铁的质量/g | 铁的形态 | c(H2SO4) /mol?L-1 | V(H2SO4) /mL | 溶液温度 | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 铁片 | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | 铁片 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 铁粉 | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | 铁片 | 1.0 | 50 | 20 | 35 | 125 |
| 5 | 0.10 | 铁片 | 1.0 | 50 | 35 | 50 | 20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将铁粉改为铁片 |
| B.向稀H2SO4中加入少量的CuSO4溶液 |
| C.向稀H2SO4中加入少量的CH3COONa固体 |
| D.向稀H2SO4中加入少量的NaOH固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com