
| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaCN | B��NaF | C��CH3COONa | D��NaNO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CH3COO������������������ | B��HSO4�� |
| C��HSO3�� | D��CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʱ��NH4Cl��Һ���� |
| B����ĭ����������������뱥��С�մ���Һ |
| C�������Ȼ�����Һ�����ˮ�Ʊ�Fe(OH)3���� |
| D�������е��ʳ��ˮ��ȡ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HA��ǿ | B��HB��ǿ | C������һ�� | D�����Ƚ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
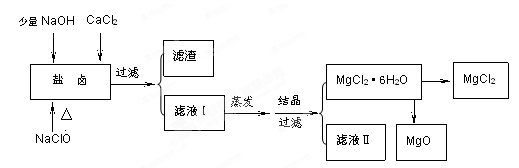

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Va>Vbʱ��c(CH3COOH)��c(CH3COO��)>c(K��) |
| B��Va��Vbʱ��c(CH3COOH)��c(H��)��c(OH��) |
| C��Va<Vbʱ��c(CH3COO��)>c(K��)>c(OH��)>c(H��) |
D��Va��Vb�����ʱ��c(K��)��c(H��)��c(OH��) ��c(CH3COO��) ��c(CH3COO��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c��R2����+ c��OH������c��Na����+c��H���� |
| B��c��R2������c��Na������c��H������c��OH���� |
| C��2c��R2����+ c��HR������c��Na��) |
| D����Ϻ���Һ�����Ϊ2aL |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com