
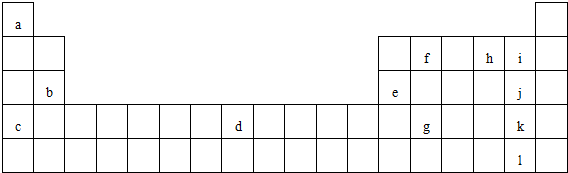
���� ����������Ԫ��A��B��C��D��E��F��ԭ��������������A��B�γ�4��ԭ�Ӻ˵ķ��ӣ�A��C�γ�3��ԭ�Ӻ˵ķ��ӣ������ַ��Ӿ�����10�����ӣ���AΪH��BΪN��CΪO��D�������ӵ��Ӳ�ṹ������ͬ������Aͬ���壬��DΪNa��E�ij��������������֣�����һ����ʹƷ����Һ��ɫ������EΪS����ԭ�������Ĺ�ϵ��֪��Fֻ��ΪCl��Ȼ����Ԫ�ص�λ�á����ʼ�����������ʡ���ѧ����������
��1������Ԫ��������=���Ӳ���������������=������������
��2��C��D���γ�ԭ�Ӹ�����Ϊ1��1�Ļ������ΪNa2O2���������Ӽ������ۼ����������̼������Ӧ��2Na2O2+2CO2=2Na2CO3+O2���ݴ˼������������
��3��O��Na��S����Ԫ�ؿ����������Ϊ8��5.75��4��ij�ֻ������N��O����N��Na����N��S��=$\frac{8}{16}$��$\frac{5.75}{23}$��$\frac{4}{32}$=4��2��1���û�����ΪNa2SO4���������ữ�������Ȼ�����Һ�����������
��4��M��һ�ֳ����Ľ������ʣ�������ת����ϵ����ͼ��ʾ��F$\stackrel{M}{��}$P$\stackrel{M}{��}$Q��MΪ��۽�������MΪFe��PΪ�Ȼ�����QΪ�Ȼ�������
��5��ʹƷ����Һ��ɫ��E��������Ϊ��������ɫ����ΪS��E��F���γ�һ����Է���������135�Ĺ��ۻ�������ӦΪS2Cl2��
��� �⣺����������Ԫ��A��B��C��D��E��F��ԭ��������������A��B�γ�4��ԭ�Ӻ˵ķ��ӣ�A��C�γ�3��ԭ�Ӻ˵ķ��ӣ������ַ��Ӿ�����10�����ӣ���AΪH��BΪN��CΪO��D�������ӵ��Ӳ�ṹ������ͬ������Aͬ���壬��DΪNa��E�ij��������������֣�����һ����ʹƷ����Һ��ɫ������EΪS����ԭ�������Ĺ�ϵ��֪��Fֻ��ΪCl��
��1��FΪCl��λ��Ԫ�����ڱ��е������ڵڢ���A���ʴ�Ϊ���������ڵڢ���A��
��2��C��D���γ�ԭ�Ӹ�����Ϊ1��1�Ļ������ΪNa2O2���������Ӽ������ۼ����������̼������Ӧ��2Na2O2+2CO2=2Na2CO3+O2����Ӧ��ת�Ƶ�����Ϊ3.01��1023�����������ʵ���Ϊ0.5mol����Ӧ�й�������������������ԭ�����ã����ݵ���ת���غ��֪��������Ϊ$\frac{0.5mol}{2}$=0.25mol������������������Ϊ0.25mol��22.4L/mol=5.6L��
�ʴ�Ϊ�����Ӽ������ۼ���5.6��
��3��O��Na��S����Ԫ�ؿ����������Ϊ8��5.75��4��ij�ֻ������N��O����N��Na����N��S��=$\frac{8}{16}$��$\frac{5.75}{23}$��$\frac{4}{32}$=4��2��1���û�����ΪNa2SO4��ʵ���Ҽ���û����������������ӵIJ����������й�ʵ�������ǣ�ȡ�������������ӵ���Һ����������ϡ�����ữ���ټ�������BaCl2��Һ�������ְ�ɫ������֤��������������ӣ�
�ʴ�Ϊ����������ϡ�����ữ���ټ�������BaCl2��Һ�������ְ�ɫ������
��4��M��һ�ֳ����Ľ������ʣ�������ת����ϵ����ͼ��ʾ��F$\stackrel{M}{��}$P$\stackrel{M}{��}$Q��MΪ��۽�������MΪFe��PΪ�Ȼ�����QΪ�Ȼ�������P��Q��Ӧ�����ӷ���ʽ�ǣ�2Fe3++Fe=3Fe2+��
�ʴ�Ϊ��2Fe3++Fe=3Fe2+��
��5��ʹƷ����Һ��ɫ��E��������Ϊ��������ɫ����ΪS��E��F���γ�һ����Է���������135�Ĺ��ۻ�������ӦΪS2Cl2����ˮ�ķ�ӦΪ2S2Cl2+2H2O=SO2��+3S��+4HCl��
�ʴ�Ϊ��2S2Cl2+2H2O=SO2��+3S��+4HCl��
���� ���⿼��λ�á��ṹ�����ʵĹ�ϵ����Ӧ�ã�Ԫ�ص��ƶ��ǽ����Ĺؼ���ע�������ʵ���������𣬣�4��Ϊ�����ѵ㣬��Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl�ȶ��Ա�HI�� | |
| B�� | CH4�ķе��NH3�ķе�� | |
| C�� | Mgʧ����������Ca�� | |
| D�� | NaCl��NH4Cl���еĻ�ѧ��������ȫ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | �������Һ | |
| A | Cu | Zn | HCl |
| B | Zn | Cu | CuSO4 |
| C | Cu | Zn | CuCl2 |
| D | Zn | Cu | H2SO4 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2Se�������⣩��H2S�ȶ� | B�� | Si��Ge���ࣩ�������뵼����� | ||
| C�� | Mg��OH��2�ļ��Ա�Be��OH��2���� | D�� | H3BO3�����ᣩ�����Ա�H2CO3��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �������ִ����Ӧ����㷺����Դ֮һ��ԭ�����һ�ֽ���ѧ��ת��Ϊ���ܵ�װ�ã���ͼ��ʾ��п��ͭ��ϡ������ɵ�ԭ����У�пƬ�Ϸ���������Ӧ�����������ԭ������ͭƬ�ϵĵ缫��Ӧʽ��2H++2e-=H2�����ܷ���ݷ�ӦNaOH+HCl=NaCl+H2O ��Ƴ�ԭ��أ�����ܡ�����ԭ���Ǹ÷�Ӧ����������ԭ��Ӧ��û�е���ת�ƣ�
�������ִ����Ӧ����㷺����Դ֮һ��ԭ�����һ�ֽ���ѧ��ת��Ϊ���ܵ�װ�ã���ͼ��ʾ��п��ͭ��ϡ������ɵ�ԭ����У�пƬ�Ϸ���������Ӧ�����������ԭ������ͭƬ�ϵĵ缫��Ӧʽ��2H++2e-=H2�����ܷ���ݷ�ӦNaOH+HCl=NaCl+H2O ��Ƴ�ԭ��أ�����ܡ�����ԭ���Ǹ÷�Ӧ����������ԭ��Ӧ��û�е���ת�ƣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μӷ�̪��Һ | B�� | ���������� | ||
| C�� | �μ���ɫʯ����Һ | D�� | �μ�̼������Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com