
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 14.5 | 29.6 | 47.4 | 77.5 | 97.9 | 551.9 | 666.8 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
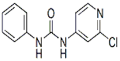
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O | 白色结晶粉末 | 170~172°C | 易溶于水 |
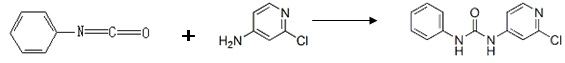
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一个D2O分子所含中子数为8 | B.NH3的结构式为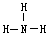 |
C.HCl的电子式为 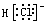 | D.沸点: HF> H2O >NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
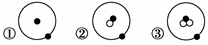
| A.a f | B.b c | C.d e | D.e f |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.随核电荷数递增,碱金属单质的熔沸点逐渐减小 |
| B.随核电荷数递增,碱金属单质的密度逐渐增大(Na、K反常) |
| C.碱金属元素包括F、Cl、Br、I、At五种元素 |
| D.碱金属元素的原子最外层都只有一个电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性强弱:HClO4>H2SO4>H3PO4 | B.离子半径:Na+>Mg2+>Al3+>F- |
| C.热稳定性:HCl>H2S>PH3>SiH4 | D.熔点:SiO2>NaCl>I2>CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com