已知A、B、C、D、E、F、G七种元素,G原子核外有四个电子层,其余原子至多只有三个电子层,且原子序数依次递增.A、B、F位于周期表的s区,A原子中电子层数和未成对电子数相同,B和A同族且位于A的下一周期,C元素基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,E的基态原子核外成对电子数是未成对电子数的3倍,F与E不同周期且F在其周期中的电负性最大,G原子d轨道有7个电子.
请回答下列问题:
(1)G基态原子的核外电子排布式是
1s22s22p63s23p63d74s2
1s22s22p63s23p63d74s2
.
(2)C、D、E的第一电离能由大到小的顺序是:
D>E>C
D>E>C
.
(3)下列有关上述元素的说法中,不正确的是
bd
bd
.(填字母)
a.B单质的熔点在同族单质中最高
b.1mol A
2E的晶体中含有4mol氢键
c.SiO
44-与FE
4-互为等电子体
d.C
3 A
6直链分子中C原子采取sp、sp
3两种杂化方式
(4)ACD分子中含
2
2
个σ键.
(5)GCl
3能与NH
3反应形成一种六配位的配合物,两个氯离子位于外界,则该配合物的化学式为
[CoCl(NH3)5]Cl2
[CoCl(NH3)5]Cl2
.
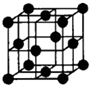
(6)C的单质是一种层状结构,B的离子位于C单质的层间、其投影位于层面内六圆环的中央,B和C 形成一种化合物,“?”表示B离子的位置,平行四边形表示在此二维图形上画出的一个晶胞.则该化合物的化学式为
LiC6
LiC6
.




 优生乐园系列答案
优生乐园系列答案

 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素. (Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答: