
 2CH3CHO+2H2O(2分)。 (3)①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出。(2分)②还原。(1分)
2CH3CHO+2H2O(2分)。 (3)①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出。(2分)②还原。(1分) NH4++OH-。氢氧化钠溶于水放热,
NH4++OH-。氢氧化钠溶于水放热,

科目:高中化学 来源:不详 题型:单选题
| | 实验操作 | 实验目的 |
| A | 向乙醚和苯酚的混合液中加入金属钠 | 确定乙醚中混有苯酚 |
| B | 向苯酚的饱和溶液中滴加稀溴水 | 制备三溴苯酚 |
| C | 将乙醇滴加到酸性KMnO4或K2Cr2O7溶液中 | 证明乙醇具有氧化性 |
| D | 将氯水加入浸泡过海带灰的溶液中 | 使溶液酸化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
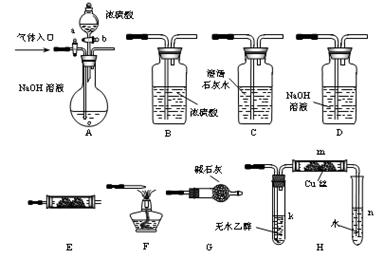
| A.在蒸发皿中灼烧CuSO4·5H2O晶体以除去结晶水 |
| B.配制0.1 mol·L-1硫酸溶液时,容量瓶应先用0.1 mol·L-1硫酸溶液润洗 |
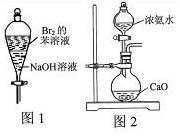
| C.用图1所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 |
| D.实验室用图2所示装置制取少量的氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
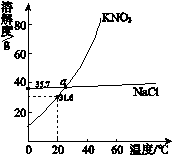
| A.40℃时,将35 g NaCl溶于100 g水中,降温至0℃时,可析出晶体 |
| B.20℃饱和KNO3溶液的溶质质量分数>31.6% |
| C.a点KNO3和NaCl溶液的物质的量浓度相等 |
| D.固体KNO3中混有NaCl,可用重结晶进行提纯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸具有强氧化性,稀硫酸无氧化性 |
| B.浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的脱水性 |
| C.稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
| D.浓硫酸与铜的反应中,浓硫酸仅表现强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的 |
| A | 向盛有1ml硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种更难溶的沉淀 |
| B | 在两支试管中分别加入相同体积相同浓度的H2O2溶液,再向其中一支试管中加入适量FeCl3溶液 | 研究催化剂对反应速率影响的 |
| C | 向沸腾的蒸馏水中逐滴滴入适量FeCl3饱和溶液,边滴边用玻璃棒搅拌,继续煮沸 | 制备Fe(OH)3胶体 |
| D | 将铜片和锌片用导线连接后同时插入稀硫酸溶液中 | 比较锌和铜的金属活泼性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com