
【题目】为了配制NH4+的浓度与Cl-的浓度之比为1∶1的溶液,可在NH4Cl溶液中加入( )
A.适量的HClB.适量的NaClC.适量的氨水D.适量的NaOH
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.3p2 表示 3p 能级有两个轨道
B.同一原子中,1s 、 2s 、 3s 电子能量逐渐减小
C.同一原子中,2p 、 3p 、 4p 能级的轨道数依次增多
D.处于最低能量的原子叫做基态原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,当线路接通时,发现M滤纸(用Na2SO4溶液的石蕊试液浸润过)的a端显蓝色,b端显红色,且知甲中电极材料是锌、银,乙中电极材料是铂、铜,且乙中两电极不发生变化。回答:
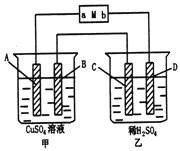
(1)甲、乙分别是什么装置?_______、________。
(2)写出A、B、C、D的电极名称以及电极材料和电极反应式。
A极:__________;B极:__________;C极:__________;D极:__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.将氯气通入石灰乳中Cl2+2OH-=Cl-+ClO-+H2O
B.碳酸钙溶于醋酸CaCO3+2H+=Ca2++CO2↑+H2O
C.钠与水反应:Na+2H2O=Na++2OH﹣+H2↑
D.向FeI2溶液中通入过量的Cl2:2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是

A. 图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0使用和未使用催化剂时,反应过程中的能量变化
B. 己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
C. 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D. 在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,下图是医院给病人输液时使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液的标签.某学生欲在实验室中配制500mL该葡萄糖注射液. 
实验用品:葡萄糖固体、蒸馏水、烧杯、容量瓶(500mL)、药匙、胶头滴管、量筒.
(1)还缺少的仪器有 .
(2)下列对容量瓶及使用的描述中不正确的是 .
A.容量瓶上标有容积、温度和浓度
B.使用前要检查容量瓶是否漏水
C.容量瓶用蒸馏水洗净后,再用5%葡萄糖注射液洗
D.配制溶液时,把称好的葡萄糖晶体小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
(3)实验中需取用固体的质量为g,该葡萄糖注射液的物质的量浓度mol/L.
(4)配制该葡萄糖注射液,下列操作会导致所配溶液的物质的量浓度偏高的是 .
A.没有将洗涤液转移到容量瓶
B.定容时俯视刻度线
C.容量瓶洗净后未干燥
D.定容时液面超过了刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是一种理想的洁净燃料,利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g) ![]() CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
CH4 | H2O | CO | H2 |
3.0 mol·L-1 | 8.5 mol·L-1 | 2.0 mol·L-1 | 2.0 mol·L-1 |
(1)则此时正、逆反应速率的关系是__________ 。(填“>”“<”“=”)
②为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/mol·L-1 | H2O初始浓度/ mol·L-1 |
1 | 360 | P | 2.00 | 6.80 |
2 | t | 101 | 2.00 | 6.80 |
3 | 360 | 101 | 2.00 | 6.80 |
(2)表中t=_________,P=_________;设计实验2、3的目的是______________;
实验l、2、3中反应的化学平衡常数的大小关系是_________(用K1、K2、K3表示)
(3)—定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物, 一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCH4、 1molH2O | amolCH4、 amolH2O、 b molCO、 c molH2 |
经测定甲容器经过5min达到平衡,平衡后甲中气体的压强为开始的1.2倍,甲容器中该反应在5min内的平均速率v(H2)=__________,若要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com