
| |||||||||||||||||||||||
(1) |
①、⑤、④、⑩、 |
(2) |
驱赶装置中的空气 |
(3) |
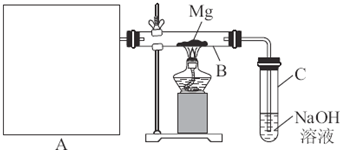
通入O2后装置D中有红棕色气体生成 |
(4) |
分离NO和NO2(或使NO2液化) |
(5) |
答案:4NO2+O2+4NaOH 精析:铜与浓硝酸反应生成的主要气体是NO2.要想证明含有NO,首先必须除去烧瓶A中的O2,因为NO接触O2就会被氧化成NO2;还要除去水蒸气,防止NO2与水反应生成NO;要证明NO的存在,必须除去大量存在的NO2气体.从气体液化温度可知,通过冰水后就能将NO2液化除去.NO为无色气体,在通过O2后有红棕色气体生成,则说明原无色气体是NO.又知NO2与N2O4存在可逆平衡关系.所以通过O2装置应用热水浴,以利于无色的N2O4转化为NO2: 2NO2 (红棕色)(无色) 若O2过量则NO、NO2气体均能被氧化为氮的最高价态,通入NaOH溶液中,被完全吸收变为硝酸钠. NO+NO2+O2+2NaOH |


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:江西省新余一中2009-2010学年高二下学期第二次段考化学试题 题型:058
二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水.
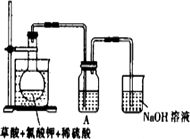
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
2KClO3+H2C2O4+2H2SO4![]() 2KHSO4+2ClO2↑+2CO2↑+2H2O
2KHSO4+2ClO2↑+2CO2↑+2H2O
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间.控制温度的目的是________________,图示装置中缺少的一种必须的玻璃仪器是________________
②装置A用于溶解产生的二氧化氯气体,其中最好盛放________(填字母).
A.20 mL 60℃的温水
B.100 mL冰水
C.100 mL饱和食盐水
D.100 mL沸水
③在烧瓶中加入12.25 g KClO3和9 g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为________
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO![]() ).饮用水中ClO2、ClO
).饮用水中ClO2、ClO![]() 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点.
①步骤1中若要量取20.00 mL水样,则应选用的仪器是________________
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
2ClO2+2KI![]() 2KClO2+I2,2Na2S2O3+I2
2KClO2+I2,2Na2S2O3+I2![]() Na2S4O6+2NaI,则步骤4中加入的指示剂为________________,滴定达到终点时溶液的颜色变化为________________
Na2S4O6+2NaI,则步骤4中加入的指示剂为________________,滴定达到终点时溶液的颜色变化为________________
③步骤5的目的是使I-将溶液中的ClO![]() 还原为Cl-以测定其含量,该反应的离子方程式为:________
还原为Cl-以测定其含量,该反应的离子方程式为:________
④若饮用水中ClO![]() 的含量超标,可向其中加入适量的Fe2+将ClO
的含量超标,可向其中加入适量的Fe2+将ClO![]() 还原为Cl-,则该反应的氧化产物为________(填化学式)
还原为Cl-,则该反应的氧化产物为________(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O| 温度 | 溶解度/g | ||
| K2CO3 | KOH | KMnO4 | |
| 20℃ | 111 | 112 | 6.38 |
| 60℃ | 127 | 154 | 22.1 |
查看答案和解析>>
科目:高中化学 来源:0103 期末题 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com