
微粒甲与离子乙在溶液中的转化关系如下图所示:微粒甲是
| A.Si | B.Na+ | C.Al | D.SO2 |
科目:高中化学 来源: 题型:单选题
A、B、C、D、E、X是中学化学中常见的物质,存在下图转化关系(部分生成物和反应条件略去)。下列推断不正确的是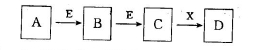
A.若D是一种强酸,则A既可以是单质,也可以是化合物,且D的浓溶液可与碳在一定条件下反应
B.若D是一种强碱,则A,B,C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某工厂用Ca SO4、NH3、HO、CO制备(NH4)2SO4,其工艺流程如下: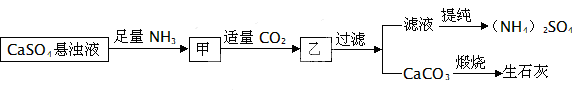
下列推断不合理的是
| A.先通二氧化碳,再通氨气,效果相同 |
| B.生成1mol(NH4)2SO4至少消耗2molNH3 |
| C.CO可被循环使用 |
| D.向甲中通二氧化碳有利于制备(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列操作和现象与结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的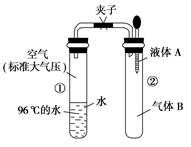
| A.氢氧化钠溶液、二氧化碳 | B.盐酸、氨气 |
| C.氢氧化钠溶液、一氧化碳 | D.石灰水、二氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列分析正确的是
| A.钠久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3 |
| B.在高温下用氢气还原MgCl2可制取金属镁 |
| C.实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3 COOH>H2CO3 |
| D.氮气的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )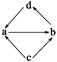
| 编号 | a | b | c | d |
| ① | Na2O | Na2O2 | Na | NaOH |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| ③ | FeCl2 | FeCl3 | Fe | CuCl2 |
| ④ | NO | NO2 | N2 | HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是( )
| A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.取少量硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
| C.取少量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取少量硫酸亚铁铵晶体放入试管中,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com