人类的生活离不开化学,生活中的化学无处不在.请回答:
(1)家用铁锅用水清洗后放置一段时间,出现红棕色的锈斑.此过程中不可能发生的变化有 (填序号).
①铁元素被氧化 ②铁元素被还原 ③铁元素由+3价转化为+2价
为防止铁锅生锈,将其洗净后,可进一步采取的措施是 (填序号).
①擦干 ②放在潮湿的地方
(2)抗酸药物的作用是中和胃里过多的盐酸.某抗酸药的主要成分是碳酸氢钠,写出碳酸氢钠与盐酸反应的离子方程式: .若此抗酸药每片含碳酸氢钠0.40g,取此药一片研碎后与足量的盐酸反应,生成气体在标准状况下的体积为 L(精确到0.01).
【答案】
分析:(1)铁锅中含有碳、铁,碳、铁和合适的电解质溶液构成原电池,较活泼的金属铁作负极,碳作正极,负极上铁失电子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定易被氧气氧化生成氢氧化铁,正极上氧气得电子和水生成氢氧根离子;
(2)碳酸氢钠和盐酸反应生成水、二氧化碳和氯化钠,根据碳酸氢钠和二氧化碳之间的关系式计算.
解答:解:(1)铁锅中含有碳、铁,碳、铁和合适的电解质溶液构成原电池,较活泼的金属铁作负极,碳作正极,铁失电子发生氧化反应,氧气得电子发生还原反应,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定被氧气氧化生成氢氧化铁,所以不可能发生的变化是②③,为防止形成原电池,要擦干,故选①;
故答案为:②③,①;
(2)碳酸氢钠和盐酸反应的离子方程式为:HCO
3-+H
+=C0
2↑+H
2O,
根据HCO
3-+H
+=C0
2↑+H
2O知,生成二氧化碳的体积=
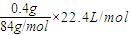
=0.11L,
故答案为:HCO
3-+H
+=C0
2↑+H
2O,0.11.
点评:本题考查了金属的腐蚀、离子反应方程式的书写、物质的量的有关计算等知识点,难度不大,离子方程式的书写是学习难点.

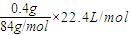 =0.11L,
=0.11L,

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 人类的生活离不开化学,拥有化学知识可以使人类生活得更加自信.
人类的生活离不开化学,拥有化学知识可以使人类生活得更加自信.