
【题目】A、B、C、D、E都是短周期的主族元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是酸性最强的含氧酸。回答下列问题:
(1)B和E分别对应的氢化物的化学式为HB、HE,氢化物的沸点HB HE(填“>”、“<”、“=”,下同) ,氢化物的稳定性HB HE。
(2)物质乙的电子式为 ;物质乙可用于呼吸面具作供氧剂,写出乙与CO2反应的化学方程式:__________ 。
(3)元素C的最高价氧化物对应水化物和D的简单阳离子按照物质的量之比为7︰2在水溶液中反应的离子方程式:_____________________________。
(4)1 mol 单质B的气体与1 mol C的氢氧化物在一定条件下恰好完全反应,生成一种盐、水及另一种气体,则所得气体的化学式为:________________ 。
【答案】(1)>(1分)>(1分);
(2)![]() (2分)2Na2O2+2CO22Na2CO3+O2(2分)
(2分)2Na2O2+2CO22Na2CO3+O2(2分)
(3)2Al3++7OH-=AlO2-+2H2O+Al(OH)3↓(2分)
(4)OF2(2分)
【解析】试题分析:D是地壳中含量最高的金属元素,则D为Al元素;E的最高价氧化物对应的水化物是酸性最强的含氧酸,则E为Cl元素;A、B、C、D、E都是原子序数依次增大的短周期的主族元素,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物,由此可得A为O元素,B为F元素,C为Na元素。
(1)HF因分子间能形成氢键,其沸点比HCl的沸点高;因F的非金属大于Cl,所以HF的稳定性大于HCl。
(2)物质乙为Na2O2,其电子式为![]() ;Na2O2与CO2反应的化学方程式为2Na2O2+2CO2 2Na2CO3+O2。
;Na2O2与CO2反应的化学方程式为2Na2O2+2CO2 2Na2CO3+O2。
(3)NaOH和Al3+按照物质的量之比为7︰2在水溶液中反应的离子方程式为2Al3++7OH-=AlO2-+2H2O+Al(OH)3↓。
(4)1 mol F2与1 mol NaOH在一定条件下恰好完全反应,生成一种盐、水及另一种气体,根据质量守恒,则所得气体的化学式为OF2。


科目:高中化学 来源: 题型:
【题目】已知反应:X+Y=M+N为放热反应,则下列说法正确的是
A.断裂X和Y的化学键所吸收的能量一定高于形成M和N的化学键所放出的能量
B.X和Y的总能量一定高于M和N的总能量
C.Y的能量一定高于N
D.因为该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.标准状况下,22.4L水的物质的量为1摩尔
B.常温常压下,32g O3气体物质的量为1摩尔
C.标准状况下,a L的氧气和氮气的混合物含有的分子数约为a/22.4×6.02×1023
D.2.24L CO2中含有的原子数为0.3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________________。
(2)下列三种情况下,离子方程式与(1)相同的是__________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
若在A项所得溶液中,继续滴加Ba(OH)2溶液,此步反应的离子方程式为:________________
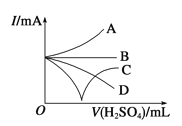
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右上图中的 曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作中正确的是( )
A.用量筒量取液体时,视线与量筒内液体凹液面最低处保持水平
B.稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌
C.用胶头滴管向试管中加入液体时,胶头滴管紧贴试管内壁
D.用托盘天平称量物质时,称量物放在右盘,砝码放在左盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属冶炼的说法正确的是
A.金属Mg只能用热还原法制备 B.高炉炼铁的原理是用CO还原铁矿石
C.电解AlCl3制金属Al D.用热还原法制金属Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从海带灰中提取碘的操作过程中,仪器选用不正确的是( )
A.称取3 g 左右的干海带——托盘天平
B.灼烧干海带至完全变成灰烬——蒸发皿
C.过滤煮沸后的海带灰和水的混合物——漏斗
D.用四氯化碳从氧化后的海带灰浸取液中提取碘——分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且![]() 的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=a mol,下列有关说法错误的是
A.若某温度下,反应后![]() =11,则溶液中
=11,则溶液中![]() =
=![]()
B.参加反应的氯气的物质的量等于![]() a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围:![]() a mol = ne =
a mol = ne = ![]() a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为![]() a mol
a mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com