
| A�������谷֮���Ա��������Ӽ����̷��У�������Ϊ�䵰���ʺ����ϸߵ�ԭ�� |
| B�������谷����̼���⡢������Ԫ�ص�������Ϊ12��1��14 |
| C��ÿĦ�������谷�����к���ԭ�Ӹ���Ϊ15NA����NA��ʾ������������ֵ�� |
| D�������谷��Ħ������Ϊ126 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������NO����0.24mol |
| B������NO2����0.26mol |
| C��ԭHNO3Ũ��Ϊ8mol/L |
| D��ԭHNO3Ũ��Ϊ2mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ʱ��Ӧ��������Һ�壬ֹͣ���ȣ�����������ʹˮ����ȫ���� |
| B�����ڵ��ھƾ��е��ܽ�ȴ����Կ��þƾ��ѵ�ˮ�еĵ���ȡ���� |
| C����Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
| D���������ʱ��Ӧʹ�¶ȼ�ˮ�����϶���������ƿ��֧�ܿ��¶���ƽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ƾ���ǿ�����ԣ���������������Һ |
| B���������л�ԭ�ԣ������������ |
| C����������������������ԣ������ڳ�ȥˮ���������� |
| D��Ũ���������ˮ�ԣ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��һ���¶Ⱥ�ѹǿ�£�����̬���������С��Ҫ�ɹ�������ķ��������� |
| B��Ħ���������Ǹ����ʵ���Է������������ԭ������ |
| C����λ���ʵ�����������ռ�������������Ħ����� |
| D��40g NaOH�ܽ���1Lˮ�У��γ���Һ���ʵ����ʵ���Ũ��Ϊ1mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
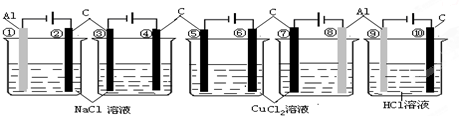
| A���ڢܢޢߢ� |
| B���٢ۢݢ�� |
| C���ڢۢܢݢޢߢ� |
| D���٢ۢݢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaHCO3��Һ�л���Na2CO3��CO2�� |
| B��NaOH���Na2O2��H2O�� |
| C��Na2CO3��Һ�л���NaHCO3��CaCl2�� |
| D��FeSO4��Һ�л���CuSO4��Fe�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol?L-1 NaHCO3��Һ��c��H+��+2c��H2CO3��=c��OH-��+c��CO32-�� |
| B��0.1mol?L-1 Na2CO3��Һ��c��Na+��+c��H+��=2c��CO32-��+c��HCO3-��+c��OH-�� |
| C��0.1mol?L-1��NH4��2Fe��SO4��2��Һ��c��SO42-����c��NH4+����c��Fe2+����c��H+�� |
| D��0.1mol?L-1 NH4Cl��Һ�У�c��NH4+����c��Cl-����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com