
 Cu+Cl2↑①
Cu+Cl2↑① 2Cu+O2↑+4H+②
2Cu+O2↑+4H+②

科目:高中化学 来源:不详 题型:填空题
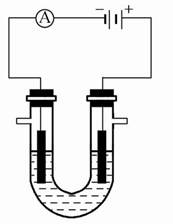
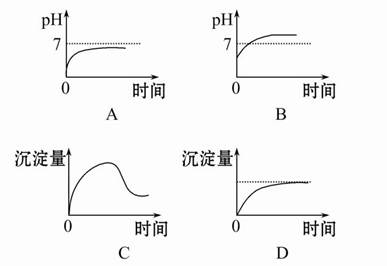
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
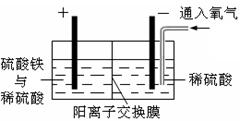
 R2Cu(有机相)+2H+(水相)分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。 Ⅳ.电解硫酸铜溶液制得金属铜。
R2Cu(有机相)+2H+(水相)分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。 Ⅳ.电解硫酸铜溶液制得金属铜。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
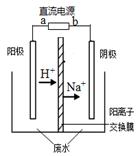
| A.若以CH4—空气燃料电池为直流电源,燃料电池的b极应通入空气 |
| B.电解过程中,阴极区Na2SO4的物质的量增大 |
| C.阳极反应CH3CHO -2e- + 2H+="=" CH3COOH + H2O |
| D.电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成Cu的物质的量是0.1 mol |
| B.转移电子的物质的量是0.2 mol |
| C.随着电解的进行溶液的pH减小 |
| D.阳极反应式是4OH--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.电路中通过电子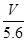 NA NA | B.n = 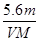 |
C.溶液中H+增加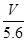 NA NA | D.n =  |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe3+ | B.Br- | C.Cu2+ | D.Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
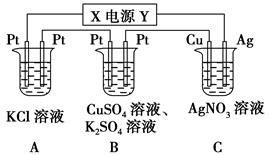
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
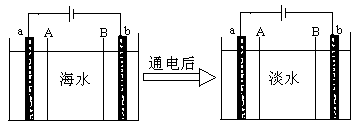
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子往a电极处运动 |
| C.通电后,a电极的电极反应式为:4OH--4e-=O2↑+2H2O |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com