
 ���ڣ�
���ڣ� 2C��g�� ��H=QkJ��mol��1��Q<0��
2C��g�� ��H=QkJ��mol��1��Q<0��
| A���٢ۢ� | B���ڢܢ� | C���٢ۢ� | D���ۢݢ� |
 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) ��H�� 0
CO(g) + H2(g) ��H�� 0  CO2(g) + H2��g�� ��H �� 0
CO2(g) + H2��g�� ��H �� 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ҫ���Ȳ��ܷ����ķ�Ӧ�����ȷ�Ӧ |
| B��ȼ�ϵ�ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ |
| C��ÿ����ѧ��Ӧ�������������ı仯 |
| D����ѧ��Ӧ�������仯�뷴Ӧ�������������������������й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 O 2��g��==H2O��g�� ��H="a" kJ��mol-1��
O 2��g��==H2O��g�� ��H="a" kJ��mol-1�� O 2��g��==H2O��l�� ��H="b" kJ��mol-1��
O 2��g��==H2O��l�� ��H="b" kJ��mol-1��| A��a<b | B��a��b��c��Ϊ��ֵ | C��a=b | D��2b=c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �ľ���ֵ����ȷ��
�ľ���ֵ����ȷ��| A��C2H5OH��l��+3O2��g��==2CO2��g��+3H2O��g������H=��1367.0 kJ/mol��ȼ���ȣ� |
| B��NaOH��aq��+HCl��aq��==NaCl��aq��+H2O��l������H=��57.3kJ/mol���к��ȣ� |
| C��S��s��+O2��g��===SO2��g������H=��269.8kJ/mol����Ӧ�ȣ� |
| D��2NO2==O2+2NO����H=��116.2kJ/mol����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
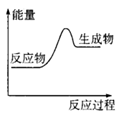
| A��þ�����ᷴӦ |
| B����ʯ����ˮ��Ӧ |
| C��̼�ڿ�����ȼ�� |
| D���Ȼ�狀������������巴Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ���Ȼ�ѧ����ʽ��ȷ���ǣ� ��
���Ȼ�ѧ����ʽ��ȷ���ǣ� ��| A��SO2(g)+KOH(aq)=KHSO3(aq)��H=-��4x-y��kJ��mol |
| B��SO2��g��+KOH��aq��=KHSO3��aq����H=-��2x-y��kJ��mol |
| C��SO2��g��+KOH��aq��=KHSO3��aq����H=-(2y-x)kJ��mol |
| D��2SO2(g)+2KOH��1��=2KHSO3��1����H=-��8x-2y��kJ��mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A�����ߴ�������ʹ���˴����ķ�Ӧ��ͼ�÷�Ӧ�����ȷ�Ӧ |
| B��E1��E2�Ǹ÷�Ӧ�ڲ�ͬ�����µĻ�ܣ�E4��E5�Ƿ�Ӧ�ڲ�ͬ�����·ų������� |
| C�����������·�Ӧ����ЧӦ��ͬ�������ߴ����ķ�Ӧ���ʽϿ� |
D���÷�Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ(ͼ�еġ�H��ʾ����1mol���������)��
PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ(ͼ�еġ�H��ʾ����1mol���������)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com