
【题目】有机物的反应往往伴随副反应发生,因此 需要分离提纯。有一种水果香精的合成步骤如下:
Ⅰ合成:
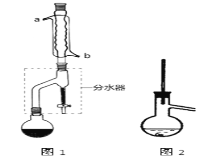
在干燥的圆底烧瓶中加入11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
Ⅱ分离提纯:
① 将烧瓶中反应后的混合物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10 mL水、10 mL 10% 碳酸钠溶液洗至中性,充分振荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥。
③ 将乙酸正丁酯粗产品转入50 mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。
主要试剂及产物的物理常数如下:
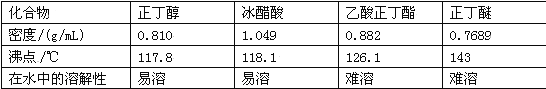
制备过程中还可能有的副反应:
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
(1)合成和分离过程中均使用沸石,其作用________________________ 。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先_______(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________杂质。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃)
C.沙子 D.石蜡油(沸点200~300℃)
(5)如何根据装置中的实验现象判断该合成反应达到了终点_______________ 。
(6)反应结束后,若放出的水为6.98 mL(水的密度为1g/mL),则正丁醇的利用率约为__________。
【答案】
(1)是防止液体加热时发生暴沸;
(2)b;
(3)过滤;正丁醚;
(4)BD;
(5)分水器中水面不再升高;
(6)88%。
【解析】
试题分析:(1)合成和分离过程中均使用沸石,其作用是防止液体加热时发生暴沸,即防止液体加热时发生暴沸;(2)冷凝管采取逆流原理通入冷凝水,其中冷水应从b管口通入,从a管中流出,有利于冷却,
故答案为:b;(3)酯层用无水硫酸镁干燥后,应过滤除去干燥剂;正丁醇和乙酸易溶于水,在用水洗、10%碳酸钠溶液洗时,已经被除去,正丁醚与乙酸丁酯互溶,水洗和10%碳酸钠溶液洗时不能除去,所以蒸馏时会有少量挥发进入乙酸丁酯,则乙酸正丁酯的杂质为正丁醚,(4)乙酸正丁酯的沸点是126.1℃,选择沸点稍高的液体加热,所以可以在甘油和石蜡油中加热,水的沸点为100℃,加热温度太低,用砂子加热温度太高不易控制;(5)合成反应中生成水,分离回流到分水器中,分水器中水面不再升高说明反应结束;(6)反应结束后,若放出的水为6.98mL(水的密度为1gmL-1),则反应生成的水为6.98mL-5.00mL=1.98mL,即1.98g,设参加反应的正丁醇为x,
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
74 18
x 1.98g
则x=(74×1.98g)÷18g=8.14g,所以正丁醇的利用率为(8.14g÷9.3g)×100%=88%。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】“神舟九号”载人飞船与天宫一号目标飞行器首次完美交会对接,标志着我国成功实现首次载人空间交会对接。“长征”系列火箭用偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体。
(1)写出该反应的化学方程式:________________________________________
(2)该反应是________(填“放热”或“吸热”)反应,反应物的总能量______(填“大于”、“小于”或“等于”)生成物的总能量,断开化学键________的总能量小于形成化学键________的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________________。
②Fe的基态原子共有________种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是__________(用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为_____,中心原子的杂化方式为________。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为690pm和780pm。则熔点:NiO________(填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为________________。
②已知该晶胞的摩尔质量为M g·mol-1,密度为d g·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是________ cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511 pm,c=397 pm;标准状况下氢气的密度为8.98×10-5 g·cm-3;储氢能力=![]() 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置制备AlC13溶液,并用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后锻烧沉淀制备新型的超导材料和发光材料七铝十二钙 (12CaO·7Al2O3)。已知A1C13易水解,易升华。
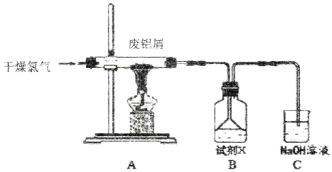
(1)①实验室用氯酸钾和浓盐酸制备氯气,其离子方程式为____________;
②C装置的作用____________;
(2)氯气与废铝屑反应生成的AlC13蒸气溶解在B中,B中盛放的试剂X是____________;为了防止AlC13蒸气凝华堵塞导管,实验中可采取的措施是____________(写出一点)。
(3)B装置中的AlC13溶液溶解CaCO3时,AlC13溶液和碳酸钙粉末的混合方式为____________;
(4)实验要控制碳酸钙和AlC13的量,要求n(CaCO3): n(A1C13)> 12:14,其原因是____________;
(5)以工业碳酸钙(含有少量A12O3、Fe2O3杂质)生产二水合氯化钙(CaC12·2H2O)的方法为:将工业碳酸钙溶于盐酸,____________。
已知:几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)

(实验中需用到的试剂和仪器有:盐酸,氢氧化钙,冰水,pH计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用碱式溴化镁废渣[主要成分为Mg(OH)Br,还含有少量有机溶剂及高分子化合物]生产C2H5Br(不溶于水,密度为1.46g/cm3)和MgCl2·6H2O,既可减少污染又可得化工原料,有关工艺流程如图所示:

回答下列问题:
(1)碱式溴化镁溶于盐酸时,1molMg(OH)Br消耗0.5mol/L的盐酸体积为_______________。
(2)分离Ⅰ操作为_______________(操作名称);分离Ⅱ操作时所需的玻璃仪器为_______________。
(3)提溴时,溶液预热至60℃时开始通入氯气,一段时间后,溶液的温度会自然升高到100℃,说明提溴反应为_______________(填“放热”或“吸热”)反应。提溴废液需减压、蒸发、浓缩的目的是_______________。
(4)在浓硫酸催化下,合成溴乙烷粗品的化学方程式为_______________;
(5)精制溴乙烷的步骤为水洗、Na2SO3溶液洗涤、水洗及干燥,其中Na2SO3溶液洗涤的目的是_______________。
(6)用惰性电极在一定条件下电解MgCl2溶液可制取催熟剂氯酸镁,该电解反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,甲醚可作燃料电池的燃料。
(1)甲醚(CH3OCH3)与 (填结构简式)互为同分异构体。
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g),反应放热。
CH3OCH3(g)+3H2O(g),反应放热。
I.一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应到达化学平衡状态的是 (选填编号,注意大小写)
a. c(H2)与c(H2O)的比值保持不变
b. 单位时间内有2molH2消耗时有1molH2O生成
c. 容器中气体密度不再改变
d. 容器中气体压强不再改变
II.温度升高,该化学平衡逆向移动后到达新平衡,混合气体的平均相对分子质量将 (填“变大”、“变小”或“不变”)
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,该燃料电池的负极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一有机物A可发生下列反应:
![]()
已知C能与NaHCO3反应产生气体,且C、E均不发生银镜反应,则A的可能结构有
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是元素周期表第ⅠA族中金属性最弱的碱金属元素。由此推断:
(1)甲元素在周期表中位置是________;
(2)甲的单质与水反应的离子方程式为____;乙单质与丙单质反应的化学方程式为_________。
(3)甲元素和丙元素的最高价氧化物对应水合物的碱性较强的是_______________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(HF)2(g) ![]() 2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
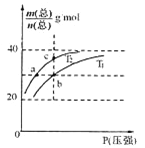
A.温度:T1< T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:v(b)>v(a)
D.当![]() 30g·mol-1时,n(HF):n[(HF)2]=2:1
30g·mol-1时,n(HF):n[(HF)2]=2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com