
分析 (1)①已知:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.5kJ•mol-1①
N2(g)+O2(g)?2NO(g)△H=+180kJ•mol-1②,
根据盖斯定律①-②×4可得:4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g),据此计算;
②根据温度对速率和化学平衡的影响分析;
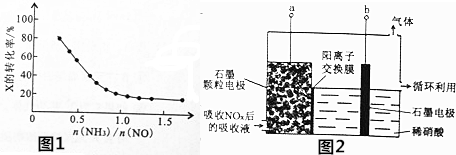
③氨气的物质的量越大,氨气的转化率越小;氨氮比增大,即氨气的浓度增大,平衡正向移动;根据氨气与氧气的反应分析;
(2)①a电极上亚硝酸失电子生成硝酸,b电极上氢离子得电子生成氢气;
②电极的面积越大,与溶液的接触越充分,电解效率越高;
③阳极上亚硝酸失电子生成硝酸.
解答 解:(1)①已知:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.5kJ•mol-1①
N2(g)+O2(g)?2NO(g)△H=+180kJ•mol-1②,
根据盖斯定律①-②×4可得:4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g)△H=(-905.5kJ•mol-1)-(+180kJ•mol-1)×4=-1625.5kJ/mol;
故答案为:-1625.5kJ/mol;
②该方法应控制反应温度在315~400℃之间,反应温度不宜过低也不宜过高,温度越高反应速率越快,温度过低,反应速率小,温度过高,使脱硝的主要反应的平衡向逆方向移动,脱硝率降低;
故答案为:温度过低,反应速率小,温度过高,使脱硝的主要反应的平衡向逆方向移动,脱硝率降低;
③氨氮比[$\frac{n(N{H}_{3})}{n(NO)}$]越大,则氨气的物质的量越大,氨气的转化率越小,由图可知,随着氨气的浓度的增大,X的转化率减小,所以X为NH3;氨氮比增大,即氨气的浓度增大,平衡正向移动,所以氨氮比由0.5增加到1.0时,脱硝主要反应的平衡将向正反应方向移动;当$\frac{n(N{H}_{3})}{n(NO)}$>1.0时,氨气与氧气的反应生成NO,所以烟气中NO浓度增大;
故答案为:NH3;正反应;过量氨气与氧气反应生成NO;
(2)①a电极上亚硝酸失电子生成硝酸,b电极上氢离子得电子生成氢气,所以a为阳极,b为阴极,则b与电源的负极相连;
故答案为:负极;
②电极的面积越大,与溶液的接触越充分,电解效率越高,所以将石墨电极设置成颗粒状的目的是增大吸收液与电极的接触面积,提高电解反应的效率;
故答案为:增大吸收液与电极的接触面积,提高电解反应的效率;
③阳极上亚硝酸失电子生成硝酸,其电极方程式为:H2O+HNO2-2e-=NO3-+3H+;
故答案为:H2O+HNO2-2e-=NO3-+3H+.
点评 本题考查了盖斯定律的应用、影响反应速率和化学平衡移动的因素、电解原理的应用,题目综合性较强,难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力,注意把握题目中所给曲线的含义.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 | |
| B. | 将溴乙烷与NaOH的乙醇溶液共热产生的气体通入溴水中,溶液褪色说明有乙烯生成 | |
| C. | 向稀氨水中滴加硝酸银溶液配得银氨溶液 | |
| D. | 溴乙烷与氢氧化钠溶液共热后,加入硝酸银溶液检验Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
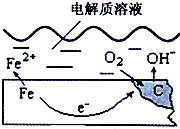 如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为:
如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=$\frac{1}{2}$Q | B. | Q1<$\frac{1}{2}$Q | C. | Q1>$\frac{1}{2}$Q | D. | Q1=Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液的pH=7 | |
| B. | 把镁粉加入FeCl3饱和溶液中,有气体和红褐色沉淀生成 | |
| C. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液蒸干的方法 | |
| D. | 盐类水解反应的逆反应是酸碱中和反应,但酸碱中和反应不一定是可逆反应. |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二上9月调研化学试卷(解析版) 题型:选择题
硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4==Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )
选 项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com