
| A、SiC(金刚砂)、SiO2 |
| B、Cu、I2 |
| C、NH4Cl、KCl |
| D、NaOH、NaCl |


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2和O2点燃生成H2O的反应与H2O电解生成H2和O2的反应 |
| B、CuSO4吸水形成晶体蓝矾与蓝矾加热失去水分生成CuSO4 |
| C、Cl2溶于水 |
| D、Na2O溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a1>a2 |
| B、a1<a2 |
| C、a1=a2 |
| D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“摩尔”是“物质的量”的单位 |
| B、1 mol O2的质量是32 g/mol |
| C、任何气体的“气体摩尔体积”均为22.4 L/mol |
| D、10 mL 2 mol/L H2SO4溶液中取出的5 mL溶液,其浓度为1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L |
| B、1 mol臭氧和1.5 mol氧气含有相同的氧原子数 |
| C、浓度均为1 mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1 |
| D、等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
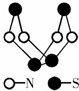 如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )
如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )| A、该物质的分子式为SN |
| B、该物质中的N原子最外层都达到8电子稳定结构 |
| C、该物质的分子中既有极性键又有非极性键 |
| D、该物质与化合物S2N2互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①③⑥ |
| C、②④⑥ | D、③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com