
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )
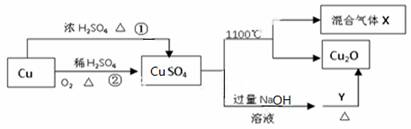
A.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体
B.Y可以是葡萄糖溶液
C.相对于途径①,途径②更好地体现了绿色化学思想
D.将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:
在下列化学方程式中,能够用离子方程式Ba2++SO42﹣=BaSO4↓表示的是( )
|
| A. | BaCl2+K2SO4=BaSO4↓+2KCl |
|
| B. | BaCO3+H2SO4=BaSO4↓+CO2↑+H2O |
|
| C. | Ba(OH)2+H2SO4=BaSO4↓+2H2O |
|
| D. | Ba(OH)2+2KHSO4=BaSO4↓+K2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期六元素A、B、C、D、E、F,原子序数依次增大;A、B的阴离子与C、D的阳离子的电子排布式均为ls22s22p6,A原子核外有2个未成对电子,C单质可与热水反应但不能与冷水反应;E、F原子在基态时填充电子的轨道有9个,且E原子核外有3个未成对电子,F能与A形成相同价态的阴离子,且A离子半径小于F离子.回答:
(1)写出各元素的符号:A ;B ;C ;D ;E ;F .
(2)写出B与C形成的化合物的电子式 .
(3)请写出基态原子F的简化电子排布式 .
(4)上述六种元素按电负性从小到大的排列是 (写元素符号).
(5)C、D、E、F元素第一电离能从小到大的排列是 (写元素符号);
(6)A、B、C、D四种元素的简单离子按半径由小到大的顺序为(用离子符号表示) .
(7)C、D、E、F四种元素中,形成的最高价氧化物对应水化物中(写化学式):酸性最强的是 碱性最强的是 .呈两性的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式不正确的是:( )
A.向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42—+20H+ = 4Fe3++3O2↑+10H2O
B.10mL0.5mol/L的明矾溶液与20mL0.5mol/LBa(OH)2溶液混合反应:
3Ba2+ + 6OH- +2Al3+ +3SO42- = 3BaSO4↓+2Al(OH)3↓
C.铜粉与63%的硝酸反应:Cu +4H++2NO3- =Cu2++2 NO2↑+ 2H2O
D.工业上用纯碱液吸收SO2:CO32-+SO2=CO2+SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
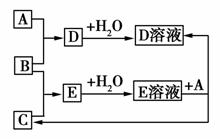
已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中不正确的是( )
A.A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B.A、B、C中三种元素形成的化合物所属物质类别一定不是碱
C.如果E溶液是一种强酸,则E溶液为盐酸
D.A、B、C中有一种金属且为A
查看答案和解析>>
科目:高中化学 来源: 题型:
央广网北京消息,据中国之声《央广新闻》报道,雾霾天气今起再次正面袭扰京津冀等地,部分地区有中到重度霾。解决环境问题需要化学知识,化学与生活联系紧密,下列说法正确的是
A.我国重点城市近年来已发布“空气质量日报”,将CO2、NO2和可吸入颗粒物等列入了首要污染物
B.PM 2.5(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶
C.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量
D.绿色化学的核心是利用化学原理对环境污染进行治理
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程属于取代反应的是( )
|
| A. | 苯与碘水混合振荡,水层颜色变浅发生萃取 |
|
| B. | 乙烯使溴水褪色 |
|
| C. | 甲烷与氯气光照下反应 |
|
| D. | 乙烯与氯化氢在一定条件下反应制取纯净的一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是 。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水。至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
[提出假设]
假设1:Fe1+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe3+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
[思考与交流]
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3 )3溶液中的Fe3+和NO
)3溶液中的Fe3+和NO 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论,并简述理由: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com