
下列除去物质杂质所选试剂或方法不正确的是
物质 | 所含杂质 | 所用试剂 | 方法 | |
A | O2 | CO2 | NaOH 溶液 | 洗气 |
B | FeSO4 溶液 | CuSO4 溶液 | Fe | 过滤 |
C | 酒精 | 水 | CaO | 蒸发 |
D | KCl | K2CO3 | 盐酸 | 蒸发 |
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是( )
A.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O AlO2- +4NH4+ +2H2O
AlO2- +4NH4+ +2H2O
B.碳酸氢铵溶液中加入足量氢氧化钡溶液: NH4++HCO3﹣+2OH- CO32﹣+ NH3·H2O + H2O
CO32﹣+ NH3·H2O + H2O
C.Cu溶液于稀HNO3:3Cu+8H++2NO3- =3Cu2++2NO↑+4H2O
D.用铜电极电解饱和食盐水:2Cl-+2H2O  Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
在恒容密闭容器中加入一定量的X并发生反应:2X(g)  Y(g),在温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示。下列叙述正确的是
Y(g),在温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示。下列叙述正确的是

A.该反应进行到N点放出的热量大于进行到W点放出的热量
B.T2下,在0 ~t1时间内,c(Y)=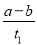 mol·L-1·min-1
mol·L-1·min-1
C.W点的正反应速率V正大于N点的逆反应速率V逆
D.W点时再加入一定量X,再达平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高三上12月月考理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列说法正确的是( )
A.在0.1molNaHSO4晶体中阳离子与阴离子总数为0.3NA
B.1.0L0.1mol·L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023
C.7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA
D.向仅含0.2molFeI2的溶液中持续通入氯气,当有0.1molFe2+被氧化时,需通入标况下C121.12L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第二次月考化学试卷(解析版) 题型:选择题
一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:
c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
D.pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:实验题
某小组以废铁屑、稀硫酸、饱和(NH4)2SO4溶液为原料,经过一系列反应和操作后,合成了浅蓝绿色晶体X.为确定其组成,进行如下实验。
Ⅰ.结晶水的测定:称取7.84g浅蓝绿晶体,加热至100℃失去结晶水,冷却至室温后,称重,质量为5.68g。
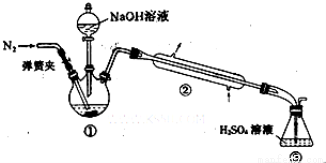
Ⅱ.NH4+的测定:将上述5.68g固体置于如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入氮气,用40.00mL 1mol•L-1的硫酸溶液吸收产生氨气。蒸氨结束后取下接收瓶,用2mol•L-1NaOH标准溶液滴定过剩的硫酸,到终点时消耗20.00mLNaOH溶液。
Ⅲ.铁元素的测定:将上述实验结束后三颈瓶中的物质全部倒入锥形瓶中,向其中加入适量3%H2O2的溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6g。回答下列问题:
(1)在实验I中,不可能用到的实验仪器是________(填正确答案标号)
A.烧杯 B.铁架台(带铁圈) C.坩埚 D.蒸发皿 E.酒精灯 F.干燥器 G.托盘天平
(2)在实验Ⅱ中,通入氮气的目的是____________。
(3)在实验Ⅱ中,用NaOH标准溶液滴定过剩的硫酸时,应使用______式滴定管;可使用的指示剂为_______;若在滴加氢氧化钠溶液时有少量待测液溅出,会使测量值________。
(4)在实验中,检验沉淀是否洗净的方法是________________。
(5)根据上述实验数据计算,该浅蓝绿晶体的化学式为_____________,三颈瓶中发生反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:填空题
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾晶体)为翠绿色晶体,溶于水,难溶于乙醇,110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。
实验室利用(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:

已知:沉淀: FeC2O4·2H2O既难溶于水又难溶于强酸
6FeC2O4+3H2O2+6K2C2O4 4K3[Fe(C2O4)3]+2Fe(OH)3↓
4K3[Fe(C2O4)3]+2Fe(OH)3↓
2Fe(OH)3+3H2C2O4+3K2C2O4 2K3[Fe(C2O4)3]+6H2O
2K3[Fe(C2O4)3]+6H2O
(1)检验硫酸亚铁铵是否变质的试剂是 ;溶解时加几滴稀硫酸的目的是 。
(2)沉淀过滤后,洗涤1的操作方法是 。
(3)在沉淀中加入饱和K2C2O4溶液,并用40 ℃ 左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40 ℃ 左右,可能的原因是 。加入30%过氧化氢溶液完全反应后,煮沸的目的是 。
(4)洗涤2中所用洗涤试剂最合适的是 (填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
用2-丙醇为有机原料制取1,2-丙二醇,其各步反应所属的反应类型是
A.氧化→加成→水解 B.消去→加成→水解
C.水解→消去→加成 D.取代→水解→还原
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
常见的无机酸25℃时在水溶液中的电离平衡常数如下表,下列选项正确的是
氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
K = 6.2×10-10 | Ka1= 4.2×10-7 | K=6.61×10-4 |
A.氟化钠溶液中通入CO2:2F-+H2O+CO2=2HF+CO32-
B.NaCN与HCN的混合溶液中:2c(Na+) = c(CN-)+ c(HCN)
C.0.2 mol•L-1 HCN溶液与0.1 mol•L-1NaOH溶液等体积混合后,溶液的pH>7
D.25℃时同浓度的NaCN和NaF溶液的pH值前者小于后者
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com