
| A. | 工业上漂白粉是由氯气和石灰乳制成的 | |
| B. | 漂白粉的主要成分是氯化钙和次氯酸钙 | |
| C. | 漂白粉漂白有色布条时,次氯酸钙直接起漂白作用 | |
| D. | 用漂白粉溶液漂白有色布条时,加些稀盐酸,漂白速率会加快 |
分析 氯气与石灰乳反应制备漂白粉,漂白粉的主要成分为次氯酸钙和氯化钙,有效成分为次氯酸钙,漂白粉与酸反应生成HClO,漂白性增强,以此来解答.
解答 解:A.因石灰乳的浓度大,则工业上漂白粉是由氯气和石灰乳制成漂白粉,故A正确;
B.氯气与石灰乳反应生成氯化钙、次氯酸钙,则漂白粉的主要成分是氯化钙和次氯酸钙,故B正确;
C.漂白粉漂白有色布条时,HClO起漂白作用,故C错误;
D.用漂白粉溶液漂白有色布条时,加些稀盐酸,易生成浓度更大的HClO,漂白速率会加快,故D正确;
故选C.
点评 本题考查漂白粉的制备及漂白原理,为高频考点,把握物质的性质、发生的反应及性质与用途为解答的关键,侧重分析与应用能力的考查,注意生成的HClO具有漂白性,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 所有化学物质内部都存在化学键 | |
| B. | 共价键存在于原子之间,也存在于分子之间 | |
| C. | 离子键是阴、阳离子之间的相互吸引力 | |
| D. | 化学键通常指的是相邻的两个或多个原子间的强烈的相互作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 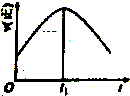 | B. | 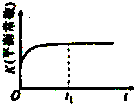 | C. | 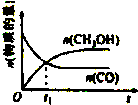 | D. | 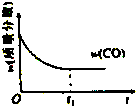 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水 | |
| C. | 用过滤的方法从碘的四氯化碳溶液中获得碘 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LBr2通入足量的NaOH溶液中生成NaBr和NaBrO,则转移电子数为0.5NA | |
| B. | 5.6gFe溶于1L0.3moL/L硝酸中,转移的电子数为0,3NA | |
| C. | 足量的Zn与浓硫酸共热可生成标准状况下的气体2.24L,则参加反应的硫酸为0.4NA | |
| D. | 标准状况下,11.2LN2和H2的混合气体中所含原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol氯气与足量水反应时转移的电子数为NA | |
| B. | 18g D2O中含有10NA个电子 | |
| C. | 50mL 18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 1mol氯气与过量铁反应时转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
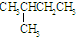 和
和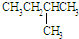
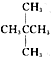 和
和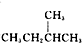
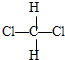 和
和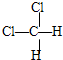
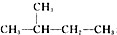 和
和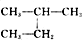
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题


 ;D的结构简式为
;D的结构简式为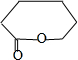 .
.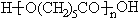 +(n-1)H2O;
+(n-1)H2O; ;
;
 写出合成该涂料的反应流程图
写出合成该涂料的反应流程图 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com