
科目:高中化学 来源:不详 题型:填空题
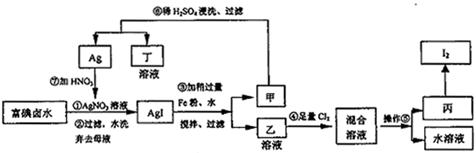
 可以循环利用的副产物是 。
可以循环利用的副产物是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
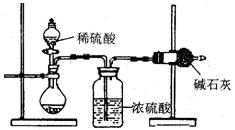
| A.装置内原有空气中的二氧化碳气体也被碱石灰吸收 |
| B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收 |
| C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收 |
| D.加入稀硫酸的量不足,则可能造成误差 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
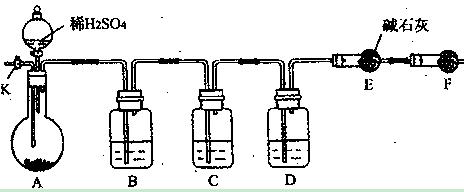
 ;
; 其作用是 ;
其作用是 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
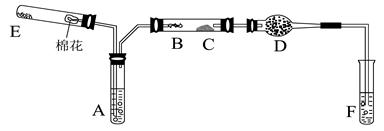
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
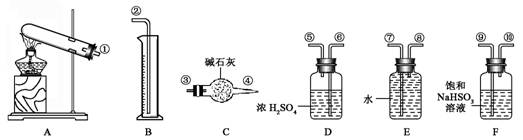
| 实验小组 | 称取CuSO4 的质量(g) | 装置C增加 的质量(g) | 量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
 都氧化了Ag。
都氧化了Ag。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
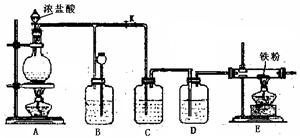
 (4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 。
(4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com